発表のポイント
- 全国の6万人以上のがん患者のがん遺伝子パネル検査1のデータベース(C-CAT データ)から遺伝子変異と患者予後などの治療成績を解析しました。
- 様々ながん種において、遺伝子の発現を誘導する重要な経路KEAP1-NRF2システムの特定の変異が、患者の予後不良、がんの悪性度と関連していることが明らかになりました。
- KEAP1-NRF2システムをターゲットとした新たながん個別化医療の開発が進むことが期待されます。
概要
KEAP1-NRF2システムは、生体内の様々な酸化ストレス2に対して遺伝子の発現を誘導する重要な経路です。一部のがん細胞では遺伝子変異によりこのシステムが異常に活性化し、がんの悪性化に関与することが知られています。しかし、その変化がどのようながん種でどのくらいの頻度で悪性化に影響するのかは不明でした。
東北大学大学院医学系研究科臨床腫瘍学分野の岩崎智行大学院生、城田英和准教授らの研究グループと東北大学東北メディカル・メガバンク機構の山本雅之教授らの研究グループは、全国のがん遺伝子パネル検査データベースであるC-CATデータを用いて、6万人以上のがん患者データを解析し、KEAP1遺伝子とNRF2遺伝子の変異分布と予後との関連を詳細に調べました。その結果、様々ながん種において、KEAP1-NRF2システムの特定の変異とがんの悪性化、患者の予後不良、化学療法抵抗性との関連を初めて明らかにしました。
これらの結果から、がん患者一人ひとりの遺伝子変異を詳しく調べることで、KEAP1-NRF2システムの異常活性化を早期に発見し、より適切な治療法を選択できる可能性が示唆されました。さらに加えてKEAP1-NRF2システムをターゲットとした新たながん治療薬の開発が進むことが期待されます。
本論文は、9月27日(日本時間)に国際学術誌Cancer Scienceに掲載されました。
詳細な説明
研究の背景
がんは、遺伝子の変化が積み重なり、細胞増殖が制御不能となる病気です。この過程で、がん細胞は周囲の環境を自分にとって有利な状態に変えていきます。具体的には、免疫細胞が集まって炎症が惹起される状態や活性酸素が増える酸化ストレス状態、酸素が不足する低酸素状態などです。さらに、抗がん剤や放射線治療などの治療も、がん細胞に強いストレスを与えます。NRF2というタンパク質は、本来、細胞を酸化ストレスから守る働きをしています。しかし一部のがんではNRF2が過剰に働いてしまい、がん細胞が治療薬に対する耐性を獲得する、腫瘍の増殖を加速させるなど、より悪性化する原因になることがわかっています。
近年、遺伝子を大規模に解析する技術が進歩し、がんの治療に遺伝子情報が活用されるようになりました。2019年から本邦でもがん遺伝子パネル検査が導入され多くの遺伝子変化を調べることで、がんの分子診断や分子標的治療薬の提案が可能になりました。患者一人ひとりに最も効果的ながん治療を行うためには、がん細胞が持つ遺伝子変異を正確に同定し、有効な治療薬を選択することが重要です。また、この検査結果はがんゲノム情報管理センター(C-CAT)で集約され、新しい薬剤や治療法の研究開発が行われています。今回の研究成果は、このデータベースを利用することによって明らかになりました。
今回の取り組み
本研究では、C-CATに保管されている60,056例の進行性または転移性固形腫瘍の日本人の遺伝子パネル検査を解析し、KEAP1およびNRF2遺伝子に変異を有するがんの分布と頻度を評価しました。また、各がんの種類と病理診断における変異状態と患者の予後との関連性についても評価しました。これらのKEAP1およびNRF2の変異は、がんの悪性度や治療抵抗性など、様々な臨床的特徴と関連しており、新たな治療標的についての洞察をもたらしました。
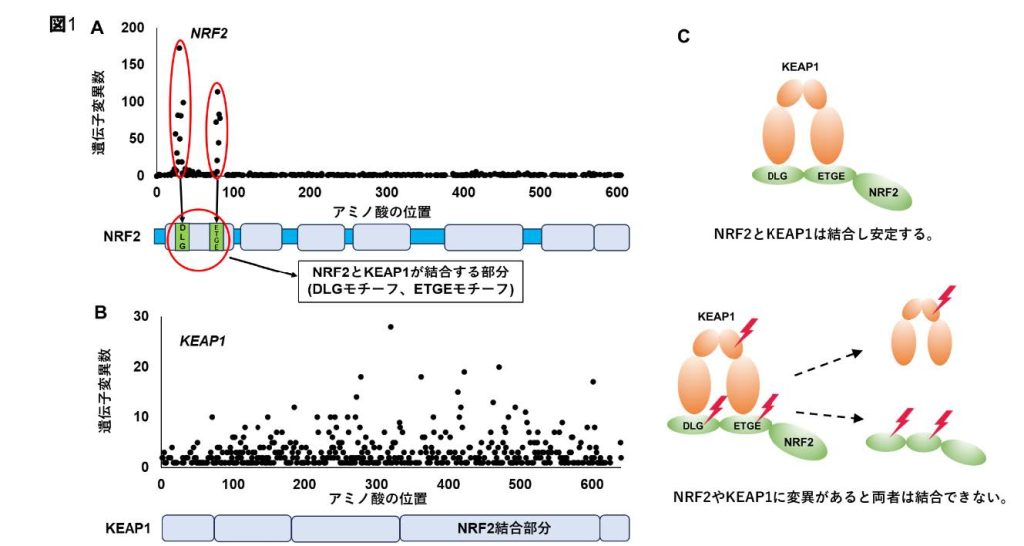
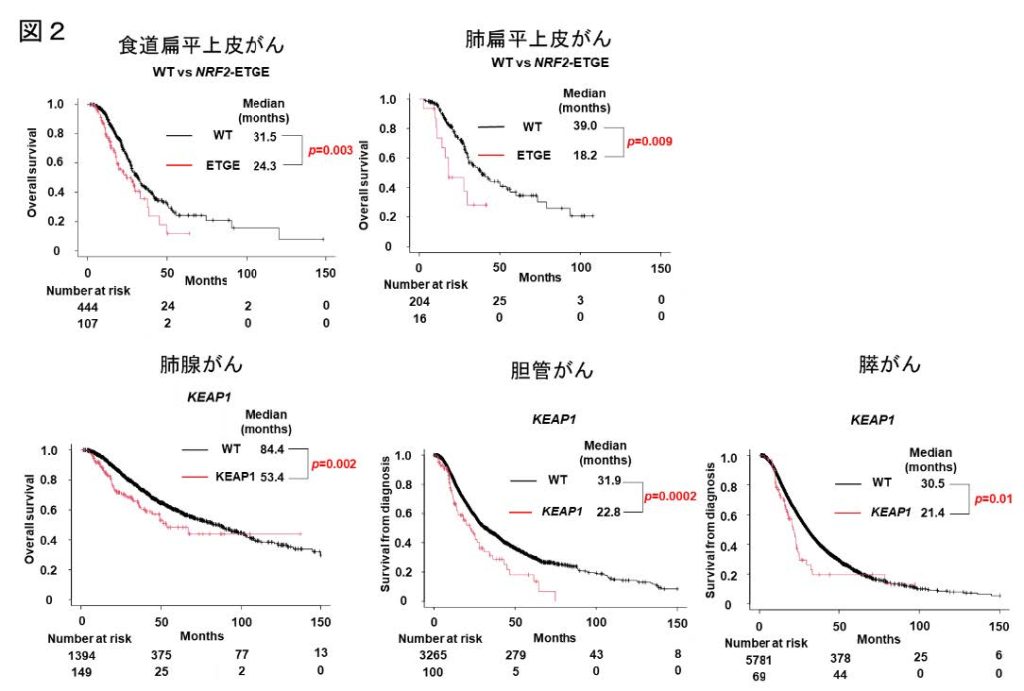
KEAP1遺伝子とNRF2遺伝子の体細胞変異は、それぞれ異なるがん種で特徴的な分布を示し、患者の予後と密接に関連していることが本研究で明らかになりました。NRF2遺伝子の変異は、ある部位に集中しており、KEAP1とのタンパク質相互作用に重要な2つのモチーフをコードする領域にホットスポットとして多く見られました(図1)。この変異は、食道扁平上皮がんの35.9%、肺扁平上皮がんでも19.6%と高頻度で検出されました。なかでも2つのうち後方のモチーフに変異を持つ扁平上皮がんにおいては、予後不良と関連していました。一方、KEAP1遺伝子の変異は全症例の2.5%と比較的低頻度でしたが、肺がんに高頻度に認められその頻度は11.0%でした。この変異を持つ患者は、変異を持たない患者と比較して有意に予後が悪いことが示されました(図2)。
米国の大規模がんゲノムプロジェクト(TCGA)データを用いた遺伝子発現解析の結果、ホットスポットに変異を有するNRF2遺伝子と、KEAP1遺伝子の変異は、それぞれ異なる遺伝子発現パターンを示すことがわかりました(図3)。
これらの結果は、KEAP1-NRF2経路の遺伝子変異が、がんの種類やその遺伝子変異の種類によって、患者の予後を大きく左右する重要な要因であることを示唆しています。
今後の展開
6万人のがん患者を対象とした遺伝子パネル検査と臨床情報の解析により、特定のがん種や病理組織型に特徴的な遺伝子変異が多数見つかりました。これらの変異と患者の予後不良、治療抵抗性との関連性については、これまでがんの治療において十分に注目されていなかった新たな発見であり、個別化医療や新たな治療法開発の可能性を示唆しています。特に、KEAP1-NRF2システムを標的とした治療戦略は、世界中の研究者の注目を集める国際的な研究課題となっています。共同研究者の東北大学東北メディカル・メガバンク機構、山本雅之教授らの研究グループは、すでにこの遺伝子に注目した薬剤を開発し、特許を取得しています。今後は、これらの薬剤の臨床試験を実施し、実用化に向けた研究開発を加速させる予定です。本研究が成功すれば、がんの個別化医療における新たなパラダイムを創出し、世界中の患者の治療に貢献できる可能性を秘めています。
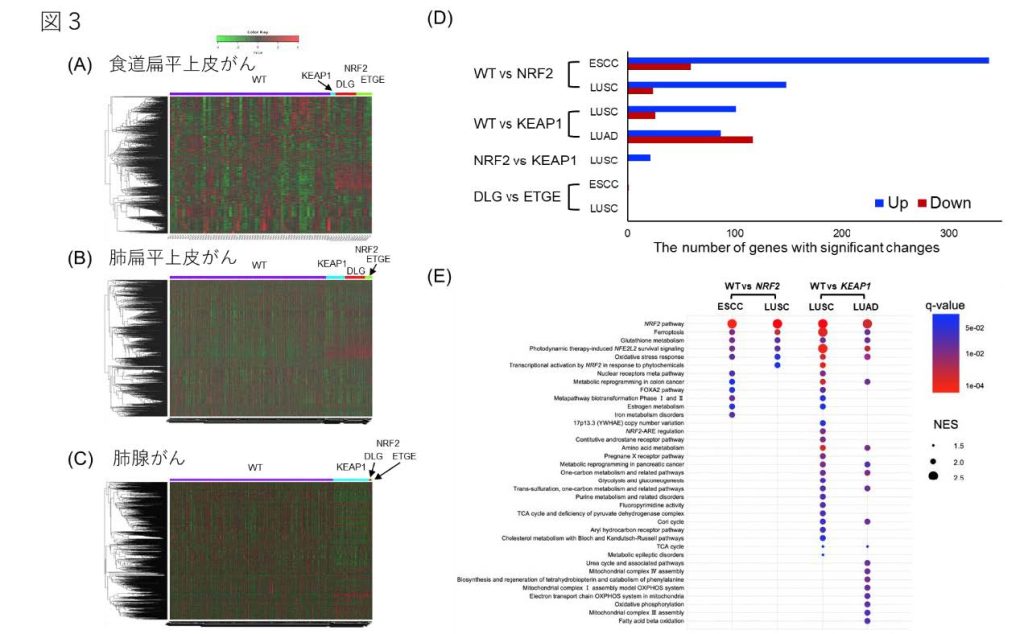
(A-C)高発現を赤色、低発現を緑色で表したヒートマップにより遺伝子発現量を可視化している
(B) KEAP1-NRF2 変異の有無もしくは変異の種類による発現変動遺伝子の数
(C)GSEA という解析手法を用いて、KEAP1-NRF2変異の有無によって発現が変動した遺伝子がどのような機能を持つか解析した結果
ESCC:食道扁平上皮がん、LUSC:肺扁平上皮がん、LUAD:肺腺がん
用語説明
- がん遺伝子パネル検査:がんの発生に関わる数百の「がん関連遺伝子」の変化を一度に調べる検査。遺伝子変化に基づいた治療を提案するために現在は保険診療で行える。 ↩︎
- 酸化ストレス:生命活動に必要な酸素呼吸の副産物として引き起こされる活性酸素などにより生体にとって有害な作用をもたらすこと。腫瘍の増殖、抗がん剤の刺激においても誘導される。 ↩︎
論文情報
タイトル:Specific cancer types and prognosis in patients with variations in the KEAP1-NRF2 system: a retrospective cohort study
著者:岩崎智行、城田英和*、佐々木啓寿、大内康太、中山勇樹、押切裕之、大槻晃史、鈴木隆史、山本雅之、石岡千加史
*責任著者:東北大学大学院医学系研究科臨床腫瘍学分野 城田英和
掲載誌:Cancer Science
DOI:10.1111/cas.16355
URL:https://onlinelibrary.wiley.com/doi/10.1111/cas.16355
問い合わせ先
(研究に関すること)
東北大学大学院医学系研究科
臨床腫瘍学分野
准教授 城田 英和 (しろた ひでかず)
TEL:022-717-8543
Email:hidekazu.shirota.e1*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学高等研究機構未来型医療創成センター
企画推進室 広報担当
教授 長神 風二 (ながみ ふうじ)
TEL:022-274-2371
Email:ingem-jimu*grp.tohoku.ac.jp(*を@に置き換えてください)
- 関連資料
- プレスリリース資料(PDF)


