がんゲノムプロファイリング検査を起点とした腫瘍由来血中循環DNAを用いた進行がんの病勢評価
2025.1.9 Thu
研究岩手医科大学医歯薬総合研究所医療開発研究部門の佐々木太雅大学院生と西塚哲特任教授、東北大学病院腫瘍内科の城田英和准教授らの研究グループは、がんゲノムプロファイリング(CGP)検査を施行した患者のデータを活用し、がん細胞由来の血中DNA(ctDNA)をデジタルPCR(dPCR)を用いて測定することで、がんの再発予測や治療効果の評価が可能であることを明らかにしました。
研究成果のポイント
本来の目的である薬剤提案に至らなかったCGP検査でも、デジタルPCRと組み合わせたctDNA測定により病勢評価(早期再発予測、治療効果判定、無増悪確証)が可能であることが確認されました。高額な臨床検査を有効に使用することにつながる成果です。
背景
我が国では悪性腫瘍(がん)により、毎年約38万人が亡くなっています(死因の第1位)。一般に切除不能な進行がんは根治療法ではなく生命予後を延長するための全身化学療法が行われます。治療薬の種類や数は罹患臓器によって決められており、治療薬の種類が少ないがんも存在します。
CGP検査は、悪性腫瘍(がん)の標準治療が終了となった、もしくは終了が見込まれる患者に次治療(治験を含む)を提案するため、保険診療としての実施が認められています。具体的には、患者のがん組織または血液を用いて、次世代シークエンシング法を用いてがんに関連する遺伝子変異を見つける方法を用います。この方法の問題点として、①1回の検査と結果説明で56万円と高額であること(3割負担で16万8千円)、②がんに関連する遺伝子が見つかったとしても次治療に到達する割合が10%以下と低いこと、③次治療の提案がない場合の検査結果の使用法がないこと、などが挙げられます。
今回、岩手医科大学附属病院で行われたCGP検査の結果を明らかにした上で、そのCGP検査を利用し、dPCRによるctDNA測定(Off The Shelf-アッセイ、以下OTS-アッセイ)を行いました(図1)。OTS-アッセイは、岩手医科大学で独自に開発されたdPCRによるctDNAの定量システムです。先行研究では、食道がん、大腸がん、尿路上皮がん、膀胱がんなどに対して、「早期再発予測」、「治療効果判定」、「無増悪確証」などについて評価可能であることが明らかになっています(Iwaya et al, Gastroenterology, 2021; Yaegashi et al, Br J Cancer, 2021; Fujisawa et al, Carcinogenesis, 2021; Tamura et al, Cancer Sci, 2024; Abe et al, J Mol Diagn, 2024)。
方法
2019年10月から2023年4月までの期間に東北大学病院個別化医療センターにCGP検査を目的に登録された岩手医科大学附属病院の患者データを用い、がんの種類、次治療が提案された割合、実際に次治療が行われた割合を調べました。
その後、OTS-アッセイに同意が得られた症例で、「早期再発予測」、「治療効果判定」、「無増悪確証」に対して臨床的妥当性の評価を行いました。「早期再発予測」は「CTなど画像検査に先だって変異アリル頻度(VAF)が上昇していること」、「治療効果判定」は、「治療内容に一致してVAFが変化すること」、「無増悪確証」は「臨床的無再発・無増殖に一致してVAF が検出感度以下を維持していること」と定義しました。
OTS-アッセイでは、CGP検査はOTS-Scanに該当します。OTS-Scanの結果から遺伝子変異を1-3個選択(OTS-Select)し、定期的採血により血液中の遺伝子変異をdPCRで定量(OTS-Monitor)しました。
結果
本研究期間中に219例のCGP検査が行われました。臓器別では、前立腺がん(12.3%)、大腸癌 (11.4%)、肺癌(8.7%)の順に多く(図2A)、遺伝子変異に紐づく次治療が提案された症例は33例(15.1%)、提案された次治療が実際に投与された割は 14例(6.4%)でした(図2B)。
dPCRによるctDNAのモニタリングを行った症例は11例(肺がん、大腸がん、胆管がん、膵がん、肛門管がん、皮膚がん、消化管間質腫瘍)であり、そのうち早期再発予測は5例(45.5%)、治療効果判定は10例(90.9%)、無再発・無増殖確証は2例(18.2%)で確認できました(図3)。全体として、11例中10例(90.9%)で、「早期再発予測」、「治療効果判定」、および「無再発・無増殖確証」のうち少なくとも一つの有効な判定が得られました。
結論
岩手医科大学附属病院でのCGP検査が次治療に結びつく割合は概ね国内他施設と同等でした。次治療提案の有無に関わらず、がんに関連する遺伝子変異が見つかっている場合には、OTS-アッセイを用いた病勢評価を行うことでゲノムデータの有効活用が可能となることが示されました。
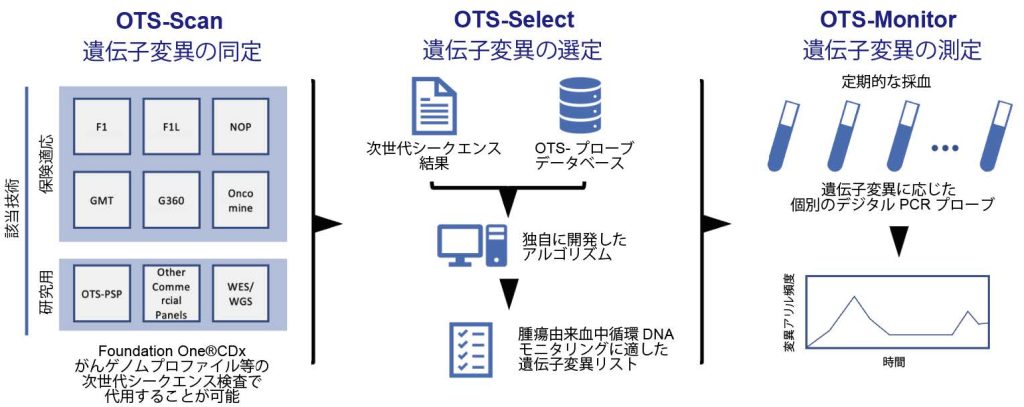
OTS-Scanでその人が持つ遺伝子変異が明らかになります。OTS-Selectでは、OTS-Scanの結果を独自に開発したアルゴリズムで解析し、ctDNAモニタリングに適した遺伝子変異をリストアップします。OTS-Monitorでは、数ヶ月ごとの定期的な採血で、OTS-Selectで選定した遺伝子変異を定量します。F1, Foundation One® CDxがんゲノムプロファイル;F1L, Foundation One® Liquid CDxがんゲノムプロファイル; NOP, OncoGuideTM NCCオンコパネルシステム; GMT, GeneMineTOPがんゲノムプロファイリングシステム; G360,Guardant360®CDxがん遺伝子パネル; OTS-PSP, Off-The-Shelf-Probes シークエンシングパネル; WES/WGS, 全エクソームシークエンス/全ゲノムシークエンス
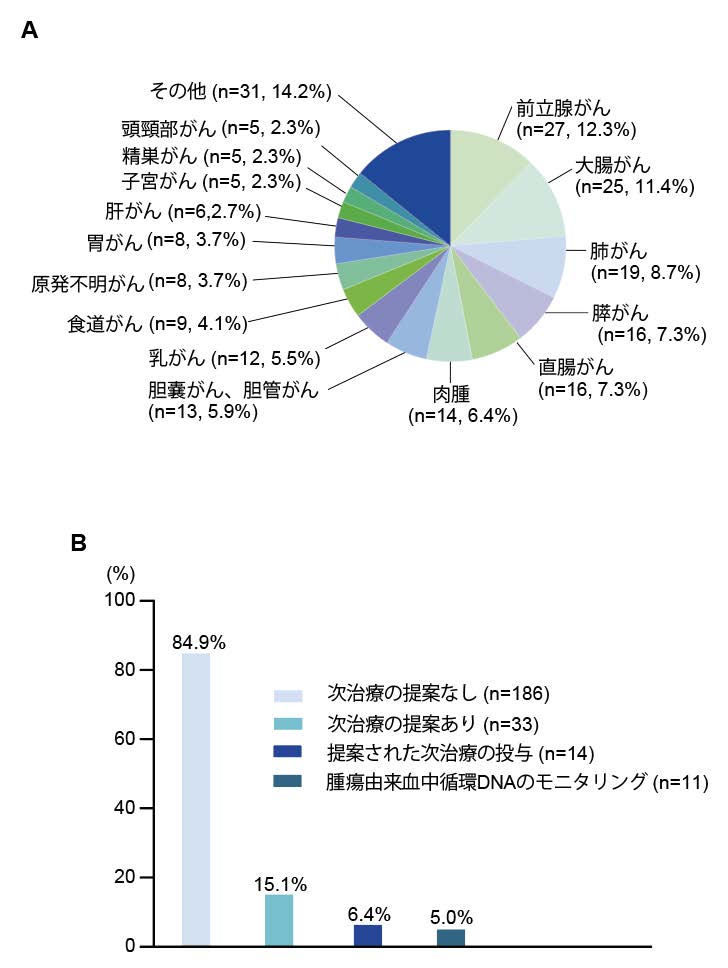
(A)がんゲノムプロファイリングを行った罹患臓器の内訳です。
(B)がんゲノムプロファイリングで次治療を提案された割合、提案された次治療が実際に行われた割合、腫瘍由来血中循環 DNA モニタリングを行った割合を示しています。
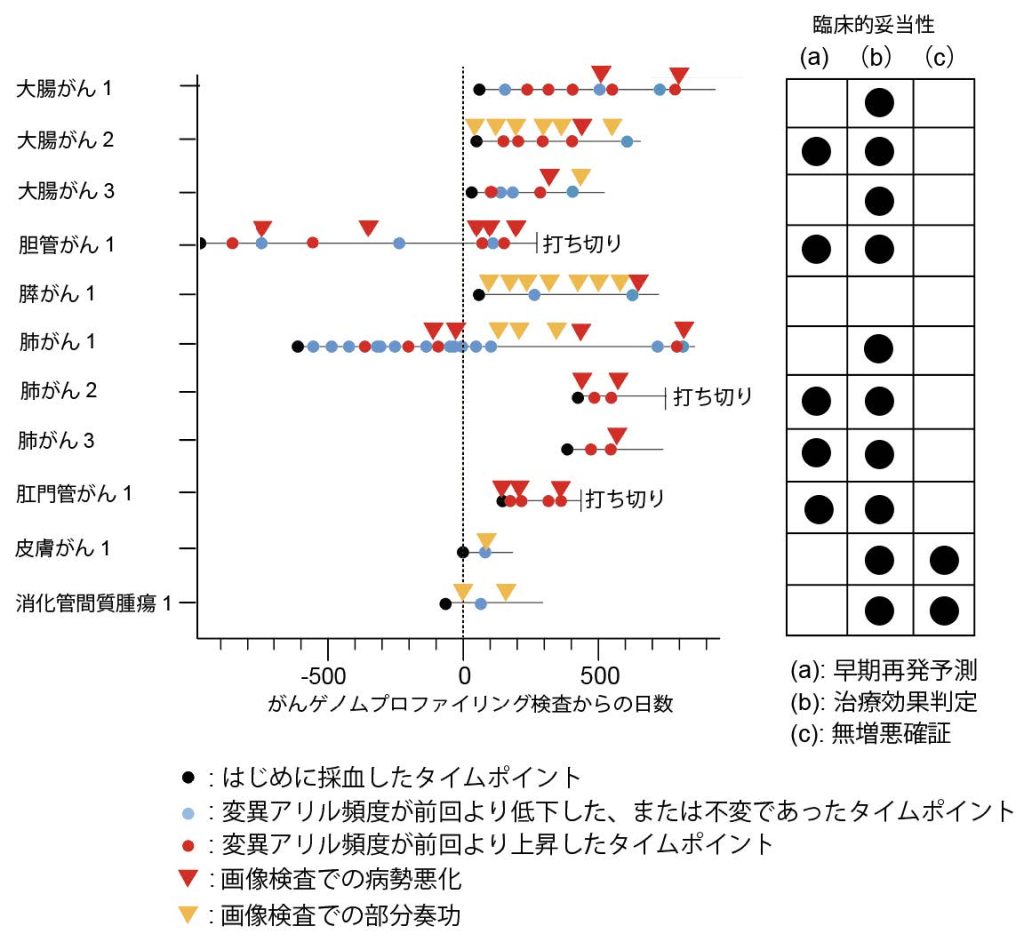
11例中10例で少なくとも一つの臨床的妥当性(早期再発予測、治療効果判定、無増悪確証)が確認されました。画像で病勢悪化が見られている症例は、VAFも上昇している傾向が読み取れます。早期再発予測が可能であった5例は、画像検査で病勢悪化が明らかとなる43日前(平均値)に変異アリル頻度の上昇が確認できました。VAFが検出感度以下(0.01%以下)であった2例は、臨床的所見を支持する無増悪確証が得られました。膵がんの1例のみ、画像での病勢悪化を確認したにも関わらずVAFが検出感度以下であり、臨床的妥当性が確認できませんでした。その要因として、膵臓由来のDNAは高度に断片化されている可能性があります。
今後の展望
- CGP検査を行ったにもかかわらず次治療の提案がなかった患者でも、OTS-アッセイを用いた病勢評価を行うことができます。
- 今回の研究ではOTS-アッセイを行った症例数が少ないため、進行がん全体の傾向を結論づけることはできませんでした。今後はより多岐にわたるがんの種類、多くの症例でOTSアッセイの臨床的妥当性を確認するための研究が必要です。
- 岩手医大附属病院では2022年4月よりOTS-アッセイを自由診療として開始しています。データを集積してより受けていただきやすい検査体制を構築します。ご興味のある方はウェブサイトをご参照ください。
研究資金
本研究は文部科学省科学研究費助成事業、日本医療研究開発機構、Quantdetect社の支援を受けて行われました。
用語解説
1.がんゲノムプロファイリング(CGP)検査:患者のがん組織または血液を用いて、次世代シークエンスを用いてがんに関連する遺伝子変異を同定する手法。悪性腫瘍(がん)の標準治療が終了となった、もしくは終了が見込まれる患者に次治療(治験を含む)を提案するため、保険診療としての実施が認められている。
2.デジタルPCR(dPCR):デジタルPCRはサンプル中に含まれる個々の分子の数をカウントして定量を行う技術で、従来のPCR法に比べ正常サンプル中に0.01%程度などのわずかに含まれる希少な分子を同定・定量することが可能な手法。
3.体細胞変異:正常な体細胞が環境要因や細胞分裂におけるDNAの複製エラーなどにより後天的に変異すること。
4.腫瘍由来血中循環DNA:がん細胞から血中遊離した、短く断片化されたDNA。
5.次世代シークエンシング:DNAを断片化し、増幅させた後に塩基配列を特定する手法。
6.変異アリル頻度(VAF):同じ位置にある遺伝子に複数の種類がある場合、その個々の遺伝子をアリルと呼び、遺伝子変異をもつアリルを変異アリルと呼ぶ。腫瘍由来血中循環DNAにおける変異アリル頻度は体内腫瘍量と関連することが知られている。
原著論文
発表雑誌名:Cancer Science
論文タイトル:Comprehensive genome profiling-initiated tumor-informed circulating tumor DNA monitoring for patients with advanced cancer(がんゲノムプロファイリング検査を起点とした進行がん患者における腫瘍由来血中循環 DNA のモニタリング)
著者:Taiga Sasaki, MD1.2., Hayato Hiraki, PhD1., Akiko Yashima-Abo, MD, PhD1., Hiromi Nagashima, MD, PhD2., Fumitaka Endo, MD, PhD3., Mizunori Yaegashi, MD, PhD4.,Shimpei Miura, MD, PhD5., Keiko Obata, PhD6., Naoki Yanagawa, MD, PhD7., Hiroaki Itamochi, MD, PhD3., Hidekazu Shirota, MD, PhD8., Takeshi Iwaya, MD, PhD3., Satoshi S.Nishizuka, MD, PhD1
DOI:https://doi.org/10.1111/cas.16446
所属:
1)Division of Biomedical Research and Development, Iwate Medical University Institute for Biomedical Sciences, Yahaba, Japan
岩手医科大学 医歯薬研究所 医療開発研究部門
2)Department of Respiratory Medicine, Iwate Medical University School of Medicine, Yahaba, Japan
岩手医科大学 内科学講座 呼吸器内科分野
3)Department of Clinical Oncology, Iwate Medical University School of Medicine, Yahaba, Japan
岩手医科大学 臨床腫瘍学講座
4)Department of Surgery, Iwate Medical University School of Medicine, Yahaba, Japan
岩手医科大学 外科学講座
5)Department of Dermatology, Iwate Medical University School of Medicine, Yahaba, Japan
岩手医科大学 皮膚科学講座
6)Department of Clinical Genetics, Iwate Medical University School of Medicine, Yahaba, Japan
岩手医科大学 臨床遺伝学講座
7)Department of Diagnostic Pathology, Iwate Medical University School of Medicine, Yahaba, Japan
岩手医科大学 病理診断学講座
8)Department of Medical Oncology, Tohoku University Hospital, Sendai, Japan
東北大学病院 腫瘍内科
Corresponding Author:Satoshi S. Nishizuka
責任著者:西塚 哲
問い合わせ先
(研究に関すること)
東北大学病院腫瘍内科
准教授 城田英和(しろた ひでかず)
TEL:022-717-8543
Email:hidekazu.shirota.e1*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院医学系研究科・医学部広報室
東北大学病院広報室
TEL:022-717-8032
Email:press.med*grp.tohoku.ac.jp(*を@に置き換えてください)
- 関連資料
- プレスリリース資料(PDF)


