日周リズムを刻む時間脳機能の解明 -世界の受け止め方と記憶の相対性を支える仕組み-
2025.11.11 Tue
研究発表のポイント
- 脳の回路応答が一日の中で変化することを、光遺伝学1を用いたラットの大脳皮質の神経刺激実験により明らかにしました。
- 覚醒・睡眠圧に関わる神経調節物質アデノシン2が、夜行性3ラットの日の出時に神経活動を抑制していることを薬理学的に示しました。
- 記憶や学習に関わる長期的増強現象(LTP)4は、日の出前には誘導可能で、同じ刺激を日没時に与えても可塑性5は生じませんでした。
- 昼行性のヒトでは時間帯が異なると考えられますが、脳内環境の日周リズムを理解することで、時間帯に応じた学習、トレーニング、リハビリ、脳刺激の最適化が期待されます。
概要
私たちは、同じ刺激を受けても、脳の状態しだいで異なる体験として捉えることがあります。
東北大学大学院生命科学研究科の道念佑樹大学院生、生駒葉子助教、松井広教授(大学院医学系研究科兼任)らは、ラットを用いて、1日の時間帯による脳内での神経信号応答の変化を世界で初めて直接観測しました。ラットは夜行性動物であり、夜間での行動が盛んです。観測により、夜が明ける頃には、眠気に関わる神経調節物質アデノシン濃度が脳内に蓄積し、神経活動が抑制されることが明らかになりました。一方で、学習や記憶に関わる神経信号の長期的増強現象(LTP)は、日の出前の時間帯にのみ誘導可能でした。この結果は、脳の興奮性や可塑性が日周リズム6によって制御されていることを示しています。昼行性であるヒトでは最適な時間帯が異なると考えられますが、大脳皮質における基本的な神経回路の動作や記憶の成立しやすさが、脳内環境の時間的変動の影響を受けている可能性を示しています。脳内環境がゆるやかな日周リズムを刻む理由を理解することで、時間帯に応じた学習、トレーニング、リハビリ、脳刺激の最適化が期待されます。
本成果は2025年10月31日付でNeuroscience Research誌に掲載されました。
詳細な説明
研究の背景
私たちの脳は、電子回路のように常に同じ反応を示すわけではありません。同じ景色を見ても感じ方は人によって異なり、心に残るかどうかもそのときの状態に左右されます。このように神経活動やメタ可塑性7(神経回路の変化のしやすさ)が変動する背景には、神経細胞を取り巻くイオンや神経調節物質の濃度変化が関係している可能性があります。
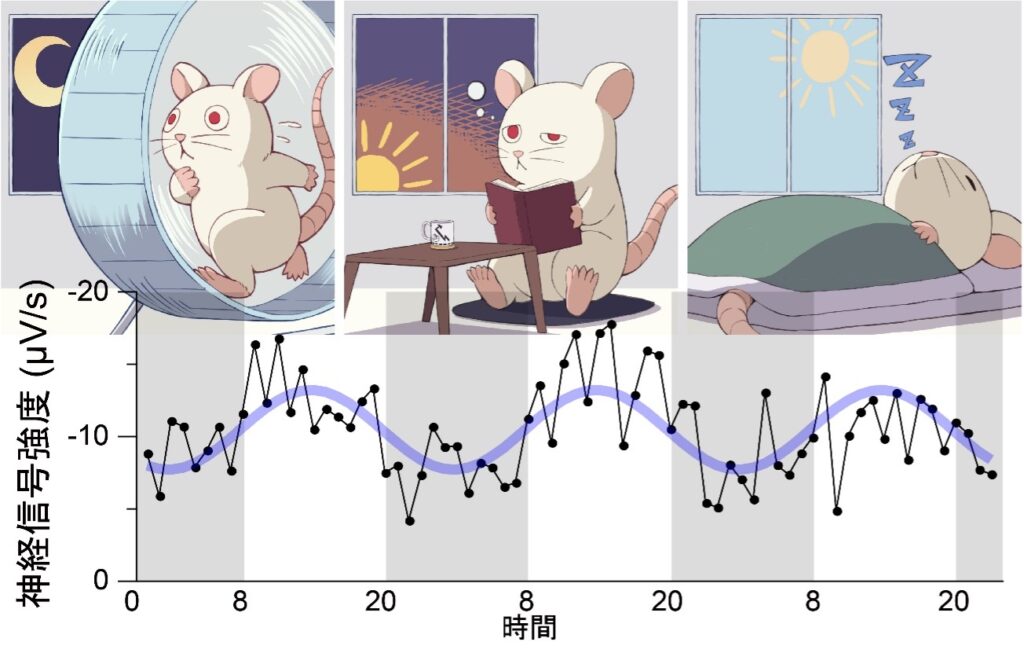
こうした脳内環境の変動の中には、24時間周期で繰り返される日周リズムに関連するものがあります。一般に「日周リズム」と呼ばれる現象のうち、体内時計によって自律的に刻まれるリズムを「概日(サーカディアン)リズム8」と呼び、昼夜の明暗変化に応じた生体反応とは区別されます。ラットは夜行性動物であり、主に夜間に活発に行動し、日の出の暁とともに活動は収まり休息に入ります。なお、ラットはヒトのように数時間連続で眠るのではなく、数十秒~数分の短い睡眠と覚醒を繰り返します。この睡眠の頻度は、昼間に高まることが知られています。この行動リズムは、体内時計による概日リズムと、外界の光環境に同調して生じるリズムの双方の影響によって形成されていると考えられます。
では、こうした日周リズムは脳内環境にどのような影響を与え、神経細胞の興奮性や可塑性の起こりやすさにどのように関与しているのでしょうか。もし時間帯によって脳内の情報処理特性が揺らぐとすれば、学習や記憶の効率にも時間依存性が存在する可能性があります。こうした「時間脳機能」の理解が進めば、学習、トレーニング、リハビリテーション、脳刺激の最適化を時間帯に合わせて行う新しいアプローチが可能になり、より効果的なパフォーマンス向上や治療応用が期待されます。
今回の取り組み
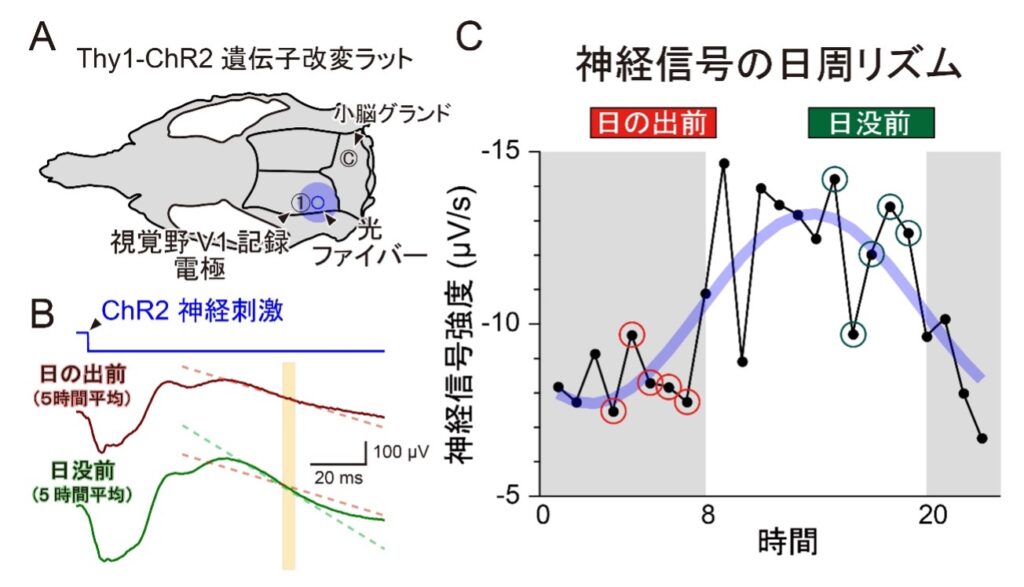
東北大学 大学院生命科学研究科 超回路脳機能分野の道念 佑樹(どうねん ゆうき)大学院生、生駒 葉子(いこま ようこ)助教、松井 広(まつい こう)教授(大学院医学系研究科、兼任)らの研究グループは、神経活動を光で制御できる遺伝子改変ラット(Thy1-ChR2ラット)の視覚野に光刺激を与え、その電気的応答(局所電位変動:LFP)9を数日にわたり連続記録しました。このラットは、藻類クラミドモナスに由来する光感受性タンパク質チャネルロドプシン-2(ChR2)10を神経細胞に発現させたモデルです。本来、哺乳類のほとんどの脳内神経細胞は光には直接反応しませんが、ChR2の発現により光照射で特異的に神経を刺激できます(光遺伝学/オプトジェネティクス)。
研究チームは、視覚情報を処理する大脳皮質視覚野(V1)11に光ファイバーを留置し、短い光パルスを照射して神経細胞を興奮させました。光ファイバー近傍の金属電極で発生する電位変動を記録し、刺激と応答を高時間分解能で計測しました。ラットは光ファイバーと電極を有線で接続したまま、回転体12を介して自由にケージ内を移動できるよう設計し、自然な行動(摂食・飲水・睡眠)を保ちながら記録を行いました。これにより、数日以上にわたる連続的かつ安定した神経活動記録が可能となり、従来30分~1時間程度に限られていた可塑性研究を大幅に拡張しました。この長期計測系を確立したことで、脳内情報処理の「日周リズム」を初めてとらえることに成功しました。
同一強度の光刺激を行った際の神経応答を比較したところ、約24時間周期で応答の強度が変動し、特に日の出前(Sunrise)では弱く、日没前(Sunset)では強いことが明らかになりました。この周期的変化には、脳の覚醒状態や内部代謝環境のリズムが関与していると考えられます。夜行性のラットは夜間に活動が高まるため、明け方には睡眠圧が上昇し、眠気に関連する神経調節物質アデノシンが脳内に蓄積していくと推測されました。
この仮説を検証するため、アデノシンA1受容体阻害薬DPCPXを投与したところ、Sunriseの時間帯では神経応答が顕著に増強されました。この結果は、明け方にアデノシン濃度が上昇して神経活動を抑制していることを示しています。つまり、アデノシンが「ブレーキ」として働き、覚醒・睡眠圧と連動して脳活動を調整していると考えられます。一方、Sunsetの時間帯ではDPCPX投与による変化はほとんど見られず、昼間の休息によってアデノシンが代謝・解消され、抑制が弱まっているためと推測されました。
神経細胞を1秒間に数十回の高頻度で数秒間刺激すると、神経応答が長期的に強化される長期増強(Long-Term Potentiation; LTP)が誘導されます。これは学習や記憶の基盤とされる現象です。本研究でも、視覚野に高頻度刺激を与えた結果、Sunriseの時間帯にのみLTP様の神経応答増強が観察されました。対照的に、Sunsetの時間帯では同様の刺激を与えてもLTPは生じませんでした。この結果は、脳の可塑性の起きやすさ(メタ可塑性)そのものが「時間帯によって制御されている」ことを初めて明らかにした重要な知見です。
本研究により、脳の神経回路応答や可塑性が一日の時間帯によって変化することが実験的に示されました。特に、夜行性動物であるラットでは、日の出前の暁(Sunrise)には神経活動が抑制され、学習・記憶の基盤となる長期増強現象(LTP)が起こりやすくなる一方で、日没前の黄昏時(Sunset)には可塑性が弱まることが明らかになりました。このリズムには、覚醒や睡眠圧と連動するアデノシンによる神経活動の抑制機構が関与しており、脳の活動状態が時間生理学的な要因によって調整されていることを示しています。本成果は、脳の興奮性や学習能力が固定的なものではなく、『時間』によって動的に変化するという新たな視点を示す成果であり、時間生物学と神経可塑性研究を橋渡しする重要な知見といえます。
今後の展望
今後は、こうした時間帯による脳機能の変動が、神経代謝・血流・グリア細胞13活動などのリズムとどのように結びついているのかを明らかにする研究が期待されます。
今回の意外な発見は、夜行性のラットにおいて、疲労が蓄積し、アデノシンによって神経活動が抑制される明け方に、むしろ神経可塑性が高まりやすい状態が生じていたという予想外の結果が得られました。一方で、昼行性であるヒトでは、夕方から夜にかけてのトワイライトゾーンの時間帯に可塑性が高まる可能性が考えられます。これを検証することで、学習やリハビリテーションにおける「最適な時間帯」を科学的に裏付ける手がかりが得られると期待されます。さらに、脳の内部環境リズムを活用して神経活動を最適化することで、時間依存的な学習支援・睡眠療法・脳刺激治療など、医療・教育・福祉分野への応用も見込まれます。
本研究は、脳が刻む「時間のリズム」を理解することにより、「いつ学ぶか・いつ刺激するか」という新たな視点から脳科学を切り開く第一歩となりました。
謝辞
本研究は、文部科学省研究費補助金JSPS KAKENHI(JP22K15218、JP24K18234、JP19H03338、JP22H02713、JP25K02373)、学術変革領域(A)「グリアデコーディング」(JP20H05896)、学術変革領域(A)「行動変容生物学」(JP23H04659、JP25H01713)、新学術領域研究「脳情報動態」(JP18H05110、JP20H05046)、東北大学国際卓越大学院プログラム Neuro Global、光科学技術研究振興財団、武田科学振興財団、上原記念生命科学財団の支援を受けて行われました。
用語説明
- 光遺伝学:光によって神経の活動をオン・オフできる技術であり、脳の信号処理や可塑性を解明する現代神経科学の主要な手法の一つである。この方法では、まず光に反応して細胞の活動を高めたり抑えたりするタンパク質を、特定の細胞に遺伝子操作で発現させる。次に、その細胞を含む組織に光を照射すると、光感受性タンパク質を持つ細胞だけが反応する。このようにして、組織全体の中から遺伝子的に区別された特定の細胞群のみを光で刺激できることから、「光(オプト)」+「遺伝学(ジェネティクス)」と呼ばれている。本研究では、ラットの脳の神経細胞にチャネルロドプシン2(ChR2)という光感受性タンパク質を発現させた。これにより、脳内に光を照射することで神経細胞のみを特異的に興奮させることが可能になった。 ↩︎
- アデノシン:脳がどれだけ活動したかに応じて蓄積し、眠気を誘うことで休息を促す「脳の疲労信号」として働く物質である。脳の神経活動が活発になると、神経細胞やグリア細胞からATP(アデノシン三リン酸)やアデノシンが細胞外へ放出される。放出されたATPは細胞外で分解されてアデノシンに変わるため、細胞外のアデノシン濃度が徐々に高まる。このアデノシンが、神経細胞に存在するA1受容体などに結合すると、神経活動が抑制的に調整される。その結果、ヒトでは日中の活動が続くほど眠気が強まり、睡眠や休息によってアデノシン濃度が低下すると再び覚醒しやすくなると考えられている。つまり、アデノシンは「脳の疲労メーター」や「睡眠圧(sleep pressure)」を示す指標のような役割を果たしている。一方、夜行性のラットでは夜間に活動が活発化するため、明け方に向けてアデノシンが蓄積すると考えられる。本研究では、このアデノシンの働きが、ラットの日の出前(Sunrise)に神経活動を抑制する要因になっていることを薬理学的に実証した。 ↩︎
- 夜行性:夜間に活動し昼間に休息する動物の生活リズムであり、ラットもこの性質を持つため、本研究では日周リズムの影響を観察するモデルとして用いられた。夜行性動物は、昼間は休息や睡眠をとり、夜になると採食・探索・社会的行動などを行う。こうした行動パターンは、体内時計(概日リズム)と光環境に応じた生理的制御によって調整されている。例えば、ラットやマウスなど多くのげっ歯類は夜行性であり、夜間に行動が最も活発になり、明け方にかけて次第に活動が低下して休息状態に入ることが知られている。 ↩︎
- 長期的増強現象(LTP):神経回路が繰り返しの刺激によって強くなる「学習と記憶の神経基盤」のことを指す。神経細胞を高頻度で刺激すると、神経細胞同士の信号の受け渡しの場であるシナプスの伝達効率が高まり、その状態が長時間持続する。この変化によって、同じ刺激に対してもより強い神経応答が得られるようになる。LTPは、脳が経験を学習や記憶として刻み込む仕組みの一つと考えられている。本研究では、この可塑性(神経の変化しやすさ)が時間帯によって変化することが明らかになった。 ↩︎
- 可塑性:神経回路が経験や活動に応じて変化し、機能を調整する性質のことを指す。「可塑(plastic)」という言葉は、形を変えられる粘土のような性質を意味し、脳が固定された構造ではなく、使われ方や刺激の種類によって神経のつながり方や強さを変えることを表している。脳の可塑性には、短期的な変化(神経活動の一時的な強弱)と、長期的な変化(シナプスの構造や機能の持続的な変化)がある。後者は学習や記憶の形成に深く関わっており、長期的増強現象(LTP)などがその代表的な例である。本研究では、この神経回路の可塑性の起きやすさそのものが、一日の時間帯によって変動することが明らかになった。これは、脳が「時間」という要素に応じて柔軟に機能を変えることを示している。 ↩︎
- 日周リズム:およそ24時間周期で繰り返される生体のリズムのことを指す。このリズムは、体温、ホルモン分泌、心拍、血圧、睡眠・覚醒のサイクルなど、多くの生理現象に現れる。日周リズムの中には、体内時計(生物時計)によって自律的に刻まれるリズムと、昼夜の明るさや温度などの外的環境に同調して生じるリズムの両方が含まれる。体内時計によるリズムを特に「概日(サーカディアン)リズム」と呼び、外界の光環境に合わせて調整されるリズムと区別される。本研究では、この日周リズムによる脳内環境の変化が、神経回路の応答や可塑性に影響することが明らかになった。 ↩︎
- メタ可塑性:神経の可塑性(つながりやすさ・変化のしやすさ)そのものが、過去の活動や状態によって変化する性質を指す。言いかえると、「可塑性の可塑性」、すなわち学習や記憶が起こりやすい“脳の状態”を調整する仕組みである。通常、可塑性は、神経細胞同士のシナプスの結合強度が変わる現象を指すが、メタ可塑性では、その可塑性を起こす“しきい値”や“方向性”(強化されるか抑制されるか)が、脳の直前の活動履歴や代謝状態によって変わる。この現象は、脳が過剰な興奮や記憶形成を防ぎ、安定性と柔軟性のバランスを保つための自己調整メカニズムと考えられている。本研究では、このようなメタ可塑性が日周リズムにより変動する可能性が示唆された。つまり、脳の「学びやすさ」自体が時間帯によって変化することを意味している。 ↩︎
- 概日(サーカディアン)リズム:外部環境に関係なく、体の内部で約24時間周期に刻まれる生物のリズムのことを指す。「サーカディアン(circadian)」という言葉は、ラテン語で「約(circa)1日(dies)」を意味する。このリズムは、脳の視交叉上核(しこうさじょうかく)と呼ばれる部位にある体内時計(生物時計)によって制御されている。体内時計は、遺伝子の発現とその抑制が一定周期で繰り返される分子メカニズムに基づいており、睡眠・覚醒、体温、ホルモン分泌、代謝、血圧など、多くの生理機能を調整している。この概日リズムは、外界の光や温度、社会的活動などの刺激(同調因子:zeitgeber)によって、地球の昼夜サイクルに合わせて微調整されている。一方で、「日周リズム」は、体内時計によるリズムと、光など外部環境による影響の両方を含むより広い概念である。 ↩︎
- 局所電位変動(LFP):脳内の多数の神経細胞が同時に活動したときに生じる電気信号を指す。脳内に電極を挿入すると、個々の神経細胞が発するスパイク(活動電位)だけでなく、神経細胞集団の同期的な電気活動によって生じる、よりゆるやかな電位の変動を記録することができる。このゆるやかな波が「局所電位変動(LFP)」である。LFPは、シナプス電流や樹状突起での電気的入力の総和を反映しており、脳領域全体の興奮・抑制のバランスや情報処理状態を知る手がかりとなる。脳波(EEG)が広い領域の活動を外部から測定するのに対し、LFPは電極先端近傍の局所的な集団活動を高精度に捉えられる点が特徴である。本研究では、ラットの視覚野(V1)に電極を設置し、光刺激に応じたLFPを長期間記録することで、脳の神経回路応答が一日の時間帯によって変化する様子を明らかにした。 ↩︎
- チャネルロドプシン-2(ChR2: channelrhodopsin-2):光に反応して細胞膜に穴(チャネル)を開けるタンパク質の一種である。もともとは、クラミドモナスという単細胞の藻類が光の方向に泳ぐために使っている光感受性タンパク質として発見された。このChR2の遺伝子を神経細胞に導入すると、その細胞は青色光を受けるだけで電気的に興奮するようになる。つまり、「光のスイッチ」で神経のオン・オフを制御できるわけである。この性質を利用した技術が光遺伝学であり、特定の神経細胞群だけを選択的に光で刺激・抑制できるため、脳の回路構造と機能を結びつけて理解するうえで革命的な手法となった。本研究では、ラットの神経細胞にChR2を発現させることで、神経細胞を特異的に刺激でき、精密な神経応答の計測が可能になり、脳活動の「日周リズム」を捉えることに成功した。 ↩︎
- 大脳皮質視覚野(V1):目から入った視覚情報を最初に処理する脳の領域である。脳の後頭部(後頭葉)に位置しており、網膜から視神経を経由して送られてくる光の情報を受け取り、その明るさ・形・位置・動きなどの基本的な特徴を解析する。この領域は視覚情報処理の入り口にあたることから「一次視覚野(primary visual cortex)」とも呼ばれる。ここで抽出された情報は、その後、色や形の認識、物体や空間の把握などを担う上位の視覚領域へと送られ、最終的に「見えた」という知覚体験へと統合される。本研究では、この視覚野V1に光ファイバーを設置し、光遺伝学的に神経細胞を刺激して電気的応答(局所電位変動:LFP)を測定することで、脳の感覚情報処理が一日の時間帯によって変化することを明らかにした。なお、本研究での「光刺激」は、遺伝子改変によってChR2を発現させた神経細胞を直接光で活性化する操作であり、網膜に光を当てて視覚入力を与える通常の「見る」刺激とは異なる点に注意が必要である。 ↩︎
- 回転体:動物の頭部に取り付けた電極や光ファイバーを外部装置につないだままでも、動物が自由に動けるようにする回転式の接続装置である。脳活動を刺激・記録する実験では、電極や光ファイバーを通して電気信号や光をやり取りする必要があるが、動物がケージ内を歩き回るとケーブルがねじれてしまう問題がある。この回転体は、ケーブルを回転軸に沿って自在に回転させることで、ねじれや張力を防ぎ、動物の自然な行動を妨げないよう設計されている。これにより、動物は装置と接続されたままでも、歩く・食べる・飲む・眠るといった通常の行動を維持することができる。本研究では、ラットの脳に光ファイバーと金属電極を設置し、それらを回転体を介して記録装置に接続することで、自然な行動状態のまま数日以上にわたる神経活動の連続記録を実現した。 ↩︎
- グリア細胞:神経細胞(ニューロン)を支え、脳全体の働きを調整する細胞群の総称である。「グリア(glia)」とはギリシャ語で「接着剤」を意味し、かつては神経細胞を支えるだけの“のり”のような存在と考えられていた。しかし近年の研究により、グリア細胞は単なる補助役ではなく、脳の情報処理や可塑性の調整に深く関わる積極的なプレイヤーであることが明らかになってきた。本研究のような「脳機能の時間変動」を理解する上で、グリア細胞は神経活動だけでなく、血流や代謝、神経修復などのリズムを媒介する重要な要素と考えられている。 ↩︎
論文情報
タイトル:Diurnal modulation of optogenetically evoked neural signals
著者:Yuki Donen, Yoko Ikoma*, Ko Matsui*
筆頭著者:東北大学大学院生命科学研究科 超回路脳機能分野 大学院生 道念 佑樹
* 責任著者:
東北大学大学院生命科学研究科 超回路脳機能分野 助教 生駒 葉子、教授 松井 広
研究室:http://www.ims.med.tohoku.ac.jp/matsui/
掲載誌:Neuroscience Research 221: 104981.
DOI:https://doi.org/10.1016/j.neures.2025.104981
問い合わせ先
(研究に関すること)
東北大学大学院生命科学研究科
教授 松井 広(まつい こう)
TEL:022-217-6209
Email:matsui*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院生命科学研究科広報室
高橋 さやか(たかはし さやか)
TEL:022-217-6193
Email:lifsci-pr*grp.tohoku.ac.jp(*を@に置き換えてください)
- 関連資料
- プレスリリース資料(PDF)
- 関連リンク
- 超回路脳機能分野


