発表のポイント
- 原発性アルドステロン症(PA)1は、脳心血管病を合併するリスクが高い高血圧疾患です。2021年にアルドステロン測定法がRIA法2から CLEIA法3に変更になりました。しかし、アルドステロン産生腺腫(APA)4を原因とするPAは手術等での治癒が可能ですが、その診断基準は未検証でした。
- APA診断基準の検証を行い、その診断においてCLEIA法がRIA法よりも優れていることを明らかにし、新たな診断基準値を確立しました。
- 手術治療等で治癒しうるAPAの見逃しが少なくなることで心臓病や脳卒中の予防につながることが期待されます。
概要
PAは一般的な高血圧と比較して脳心血管病の発症リスクが2~4倍とされています。PAはAPAと呼ばれる腫瘍が原因である場合、腹腔鏡手術で摘出したり、ラジオ波焼灼術で腫瘍を焼き切ったりすることで治癒し、高血圧も解消されます。APAを診断するためには、副腎静脈サンプリング(AVS)5という比較的大がかりなカテーテル検査によって判定されます。近年アルドステロン測定法がRIA 法から CLEIA法に変更されました。それ以降、AVSを行うための基準の検証は行われておらずAPAを見逃してしまう可能性がありました。
東北大学病院糖尿病代謝・内分泌内科の小野美澄助教と東北大学大学院医学系研究科佐藤文俊客員教授らのグループは、CLEIA法のAPA診断について検証を行い、CLEIA法のAPA診断能はRIA法に比較して優位に高いことを明らかにし、新たな診断基準値を確立しました。本研究は、富士レビオ株式会社との共同研究として実施されました。本研究成果は米国内分泌学会誌Journal of the Endocrine Societyにて2024年4月20日にオンライン公開されました。
詳細な説明
研究の背景
全国で4300万人いるとされる高血圧症患者の約10%が、PAが原因とされています。PAとは、副腎という腎臓の上に位置する臓器においてアルドステロンという血圧上昇ホルモンが過剰に分泌されることで、高血圧や体内ミネラルの一種であるカリウムの血中濃度が低下する疾患です。高血圧症は、心不全や心筋梗塞、脳卒中の強力な発症リスク因子です。その中でもPAは一般的な高血圧(本態性高血圧)と比較して心血管病の発症リスクが2~4倍とされています。高血圧診療においてはPAの早期発見と適切な治療により、脳卒中や心臓病、慢性腎臓病などの合併症が進行を予防することが可能となりますが、実際の診療ではPAが見逃されることが多いのが現状です。
さらに、PAは左右2つの副腎が同程度のアルドステロン分泌をする場合(両側性病変)と、左右2つの副腎のどちらか片方のみが過剰にアルドステロン分泌をする場合(片側性病変・BHA)に大別されます。片側性病変のほとんどはAPAと呼ばれる腫瘍が原因で、APAのある側の副腎を腹腔鏡手術で摘出したり、近年開発されたラジオ波焼灼術で原因部位を焼き切ったりすることで、アルドステロン過剰分泌が治癒し、高血圧を根治もしくは改善することができます。
APAを診断するためにはいくつかのプロセスが必要となりますがその中でもAVSというカテーテル検査によって、左右2つの副腎のアルドステロン分泌度合いの差を調べ、手術治療あるいはラジオ波焼灼術の適応があるかを決定します。AVSは大学病院のような限られた医療機関でしか実施できない検査であり、なるべくAPAである事前確率を高める必要があります。
PAであるかどうかは血液中のアルドステロンや腎臓からのレニン6の基礎値測定を行い、その後、機能確認検査(カプトプリル負荷試験や生理食塩水負荷試験など)で確定診断を行います。2021年にアルドステロン測定方法がRIA法からCLEIA法に変更となり、新測定法での新たなPA診断基準について東北大学でも検証してきました(参考文献1)。しかしPAを含む高血圧症患者の中から、手術等で治癒し得るAPAを見つけるためのスクリーニング基準については明らかでなく、CLEIA新測定系での検証が求められていました。
今回の取り組み
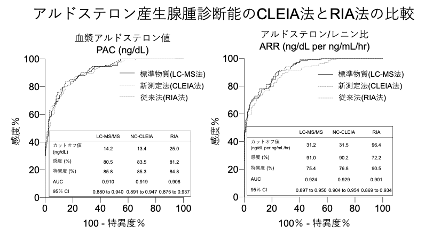
今回、東北大学病院糖尿病代謝・内分泌内科の小野美澄(おの よしきよ)助教、手塚雄太(てづか ゆうた)助教、東北大学大学院医学系研究科佐藤文俊(さとう ふみとし)客員教授らのグループは、東北大学病院で診療を受けたPAを含む高血圧症患者の計344名分の検体を使用して、APA診断のためのPAC(単位ng/dL)及びPAC/血漿レニン活性比(ARR:単位ng/dL per ng/mL/hr)7カットオフ値についてCLEIA、RIAの各測定法の受信者操作特性曲線(ROC)8とROC曲線下面積(AUC)9解析により検証しました。その結果、PACにおけるAPA診断カットオフ値はCLEIA:13.4(AUC0.919, 感度83.5%, 特異度85.3%)、RIA:25.0(AUC0.906, 感度81.2%, 特異度84.8%)であり、ARRでのAPA診断カットオフ値はCLEIA:31.5(AUC0.929, 感度90.2%, 特異度76.8%)、RIA:96.4(AUC0.901, 感度72.2%, 特異度90.5%)であり、PACとARRいずれもRIA法に比較してCLEIA法のAPA診断能は優位に高いことが示されました(図1)。
また、CLEIA法におけるAPA診断能について感度を100%とした場合、PACで6.0、ARRで15であり、これらの基準値を上回る際には積極的にAVSを行うことにより多くのAPAの見逃しを防ぎ得ることが示唆されました。
今後の展開
原発性アルドステロン症は心血管病や脳卒中のリスクが高い二次性高血圧症のひとつですが、その中でもアルドステロン産生腺腫が原因の場合は手術もしくはラジオ波焼灼術で治癒する見込みがあります。今回の研究結果を受けて、副腎静脈サンプリングを行わねばならない基準を示すことによって、より多くの治癒すべき患者の見逃しを防ぎ、将来の心血管病や脳卒中のリスクを低下させ、より良い健康的な生活ができるようになることが期待されます。
参考文献
1.Tezuka Y.et al. Hypertens Res. 2024
用語説明
- 原発性アルドステロン症(PA):副腎という左右2つ存在する臓器から分泌される血圧上昇ホルモン、アルドステロンが、自律的かつ過剰に分泌されることで起こる疾患。アルドステロンの作用によって血圧が上昇し、尿中へのカリウム排泄が亢進することで低カリウム血症を来す。また、アルドステロンは動脈の炎症を惹起し、動脈硬化やそれに伴う心筋梗塞、脳梗塞などの心血管病を引き起こす。 ↩︎
- RIA法:放射免疫測定(radioummunoassay)の略。RIA法は、アルドステロン測定法の一つであり、放射能を利用する。日本では2020年度までRIA法でアルドステロンが測定されてきた。 ↩︎
- CLEIA法:化学発酵酵素免疫測定(chemiluminescent immunoassay)の略。アルドステロン測定法の一つであり、抗体と抗原の結合反応に由来する光を利用する。以前からアルドステロンの測定に用いられていたが、より精度の高いCLEIA法が2019年頃に開発され、2021年度以降の原発性アルドステロン症診療に用いられている。 ↩︎
- アルドステロン産生腺腫(APA):副腎に発生するアルドステロン過剰分泌をする腫瘍で、通常左右どちらか片方に認める。APAである場合は病変のある副腎を手術もしくはラジオ波焼灼術を行うことでPAは治癒する。 ↩︎
- 副腎静脈サンプリング(AVS):鼠径部(腿の付け根)から静脈に細い管(カテーテル)を入れて左右の副腎静脈から採血をして、左右それぞれの副腎からどのくらいアルドステロンが分泌されているのかを調べる検査。一定の基準で左右差がある場合はAPAと診断できる。 ↩︎
- レニン:体内の水分量や塩分量、血圧のバランスを保つために、腎臓から分泌されるホルモン。レニンは、アンジオテンシンというホルモンを介して、アルドステロンの分泌を促す。原発性アルドステロン症では、アルドステロンが過剰に分泌されているため、レニンの分泌は抑制される。 ↩︎
- アルドステロン・レニン比(ARR):原発性アルドステロン症のスクリーニング、診断の際に基準となる血液中のアルドステロン値をレニン値で割った値。 ↩︎
- 受信者操作特性曲線(ROC):診断テストや分類器の性能を評価するためのグラフで、縦軸に「真陽性率(感度)」、横軸に「偽陽性率」をプロットし、各ポイントは異なる閾値に対応する。 ↩︎
- ROC曲線下面積(AUC):ROC曲線の下にある面積を示す指標で1に近いほど診断能が高いことを示す。 ↩︎
論文情報
タイトル:Screening Cutoff Values for the Detection of Aldosterone Producing Adenoma by LC-MS/MS and a Novel Non-competitive CLEIA
著者:*Yoshikiyo Ono, Yuta Tezuka, Kei Omata, Ryo Morimoto, Yuto Yamazaki, Sota Oguro, Kei Takase, Akihiro Ito, Tatsunari Yoshimi, Satoshi Kojima, Sadayoshi Ito, Hironobu Sasano, Takashi Suzuki, Tetsuhiro Tanaka, Hideki Katagiri, and Fumitoshi Satoh
*責任著者:東北大学病院糖尿病代謝・内分泌内科 助教 小野美澄
掲載誌:Journal of the Endocrine Society
DOI:https://doi.org/10.1210/jendso/bvae080
URL:https://academic.oup.com/jes/advance-article/doi/10.1210/jendso/bvae080/7655430?utm_source=authortollfreelink&utm_campaign=jes&utm_medium=email&guestAccessKey=5e645779-fd3f-4d81-ad31-f71bc9220c60
問い合わせ先
(研究に関すること)
東北大学病院糖尿病代謝・内分泌内科
助教 小野 美澄(おの よしきよ)
TEL:022-717-7779
Email:yoshikiyo.ono.e5*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学病院広報室
東北大学大学院医学系研究科・医学部広報室
TEL:022-717-8032
Email:press*pr.med.tohoku.ac.jp(*を@に置き換えてください)
- 関連資料
- プレスリリース資料(PDF)
- 関連リンク
- 糖尿病代謝・内分泌内科学分野 糖尿病代謝・内分泌内科


