細胞死の新たなバイオマーカーを発見!―フェロトーシス細胞でのビリベルジン動態を計測―
2024.10.8 Tue
研究発表のポイント
- 鉄依存性の細胞死であるフェロトーシス1時に細胞内のビリベルジン2量が減少することを、シアノバクテリア(ラン藻)3由来の光受容体タンパク質 (シアノバクテリオクロム) 4を用いて発見しました。
- ビリベルジンの減少は、フェロトーシスに特有の現象であることが分かりました。
- シアノバクテリオクロムによるビリベルジン測定は、フェロトーシスの新たなバイオマーカー5として、がん治療の効果や感受性の判定に役立つことが期待されます。
概要
ラン藻由来のタンパク質が、がん治療の効果判定の鍵になる可能性を発見しました。フェロトーシスは 2012年に報告された鉄依存性の細胞死で、生体内でがん細胞の除去機構として働くことが分かっています。また化学療法や免疫療法によってがんが縮小する際にフェロトーシスが起きることも明らかになっています。
東北大学大学院医学系研究科生物化学分野の西澤弘成非常勤講師、中嶋一真(現平鹿総合病院)、五十嵐和彦教授らと東北大学加齢医学研究所分子腫瘍学研究分野の田中耕三教授らの研究グループは、東京都立大学の成川礼准教授との共同研究により、シアノバクテリア由来の光受容体タンパク質であるシアノバクテリオクロムを用いて、フェロトーシス時に細胞内のビリベルジン量が大きく減少することを突き止めました。これはフェロトーシス特有の現象であり、ビリベルジンがフェロトーシスのバイオマーカーとして、将来、がん治療の効果や感受性の判定に利用できる可能性を示すものです。
本研究の成果は、2024年9月28日に日本生化学会英文誌 The Journal of Biochemistryにオンライン掲載されました。概要はYouTubeの医学系研究科生物化学分野チャンネルでもご覧いただけます。
詳細な説明
研究の背景
フェロトーシスは2012年に報告された鉄依存性の細胞死のことで、生体内でがん細胞を取り除く役割が明らかになっており、近年注目されています。しかし、フェロトーシスが起きたことを示す絶対的なバイオマーカーは確立されておらず、特に臨床現場でがんの治療効果や感受性の判定に使えるものはありませんでした。
今回の取り組み
東北大学大学院医学系研究科生物化学分野の西澤弘成(にしざわ ひろなり)非常勤講師、中嶋一真(なかじま かずま)学士 (現 平鹿総合病院)、五十嵐和彦(いがらし かずひこ)教授の研究チームは、東京都立大学の成川礼(なりかわ れい)准教授らが開発した、ビリベルジンと結合して赤色蛍光を発するシアノバクテリオクロム (参考文献1) を用いて、フェロトーシスを誘導された細胞でビリベルジン量が大きく減少することを突き止めました(P = 2.0 x 10–6)(図1)。さらに、東北大学加齢医学研究所分子腫瘍学研究分野の田中耕三(たなか こうぞう)教授らとの共同研究によって、ビリベルジンが減少する様子を動画で記録することにも成功しました。
このビリベルジンの減少は、アポトーシス6やネクロプトーシス7などの他のタイプの細胞死では起こらず、フェロトーシスに特有の現象であることもわかりました。さらに、研究チームが作製した、転写因子8BACH19の再発現によるフェロトーシスモデル細胞(参考文献2) において、細胞内ビリベルジン動態を調べたところ、フェロトーシス誘導開始前からビリベルジン量が低下しており、フェロトーシスが誘導されるとさらに減少することがわかりました(P = 0.043)(図2)。ビリベルジン量の低下が、潜在的なフェロトーシスへの待機状態を示している可能性があり、フェロトーシスへの感受性の指標にもなり得ると考えられます(図2)。
これらの結果は、将来的にこのシアノバクテリオクロムを用いて生きた細胞内のビリベルジンを検出することで、フェロトーシスを利用したがん治療の効果や感受性を判定できる可能性を示しています。
今後の展開
現在のがん化学療法の主役は分子標的治療10ですが、これらの治療が効かなくなったがん細胞では、フェロトーシスへの感受性が上がることがわかっています。研究チームは、このがん細胞の変化(治療への耐性化)を本研究の手法を用いて検出することができないか検討しています。これが実現すれば、がん臨床の現場で、早期に耐性化や治療効果を予測し、より適切な治療選択を迅速に行うための診断法の開発につながると考えられます。
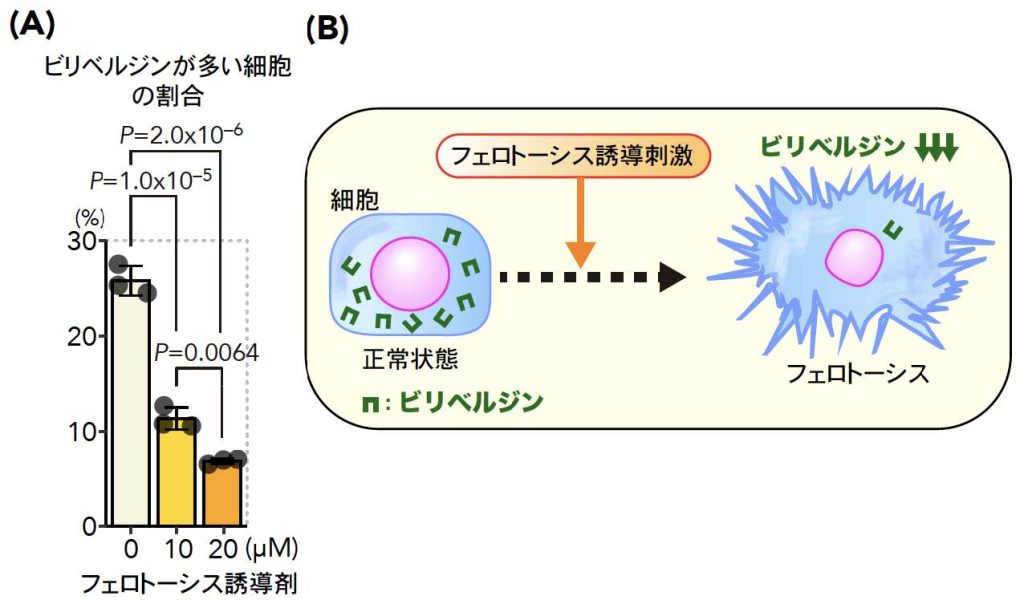
図1.フェロトーシス誘導時に細胞内ビリベルジンが減少する
(A) シアノバクテリオクロムで細胞内のビリベルジン量を測定した。フェロトーシス誘導剤の投与によって、ビリベルジンが多い細胞の割合が減少した。論文内では細胞内ビリベルジン量の平均値が下がることも示している。
(B) 概念図
細胞にフェロトーシス誘導刺激を加えると、細胞死 (フェロトーシス) が起きるとともに細胞内ビリベルジンが大きく減少する。
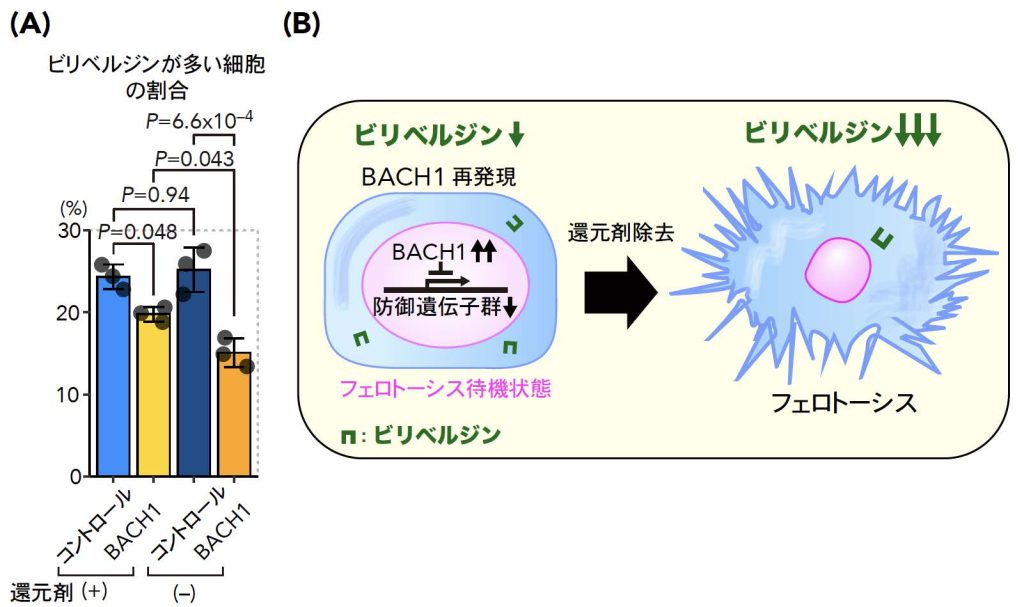
図2.BACH1 再発現によるフェロトーシスモデル細胞では、フェロトーシス誘導前から細胞内ビリベルジンが減少している
研究チームは以前、フェロトーシスの強力な促進因子であるBACH1を再発現させることでフェロトーシスに対する防御遺伝子の転写を抑制し、フェロトーシスを誘導できるモデル細胞を作製した (参考文献2)。この細胞では培養液中の還元剤を取り除くことで自動的にフェロトーシスが誘導される。
(A) 還元剤の存在下 (フェロトーシス誘導前) でもすでに細胞内ビリベルジン量が低下しており、それが還元剤の除去によって更に減少した。
(B) 概念図:フェロトーシス誘導前から細胞内ビリベルジンが減少していることは、これらのモデル細胞が潜在性にフェロトーシス待機状態にあることを示唆しており、ビリベルジン量を測ることで細胞のフェロトーシス感受性を予測できる可能性がある。
謝辞
本研究は、日本学術振興会科学研究費補助金(研究代表者:西澤弘成(JP23K14556, JP20K16296, JP19K23738)、松本光代(JP23K24156,JP22H02895, JP19K07680)、五十嵐和彦 (JP22H00443, JP20KK0176,JP18H04021)、東北大学大学院医学系研究科若手共同研究奨励研究費(研究代表者:西澤弘成)、艮陵医学振興会研究助成金(研究代表者:西澤弘成)、武田科学振興財団医学系研究助成金(研究代表者:西澤弘成)、孫正義財団助成金(研究代表者:山中美慧)、カシオ科学振興財団助成金(研究代表者:五十嵐和彦)、三菱財団助成金(研究代表者:五十嵐和彦)の支援を受けて行われました。
用語説明
- フェロトーシス:2012年にDixonらによって新しく報告された細胞死機構。細胞内自由鉄(Fe2+)を触媒として細胞膜リン脂質の過酸化反応が連鎖し脂質ヒドロキシラジカルが蓄積することで細胞が死に至ると考えられています。自由鉄を除去する鉄キレート剤の投与によって抑制されます。 ↩︎
- ビリベルジン:赤血球の主成分であるヘモグロビンの分解で生じる生成物。このビリベルジンがさらにビリルビンに変換され、肝臓に取り込まれ修飾されてから胆管を経て消化管に排泄されます。ビリベルジンには光を吸収する作用や還元作用、抗炎症作用もあることがわかっています。 ↩︎
- シアノバクテリア:光合成を行う細菌の一種。水中や湿潤な環境に広く分布し、以前はラン藻とも呼ばれていました。 ↩︎
- シアノバクテリオクロム:シアノバクテリアが発現する光受容体タンパク質。この光受容体によって、シアノバクテリアは可視光を検知し、光合成などの細胞内機能を調節することができます。 ↩︎
- バイオマーカー:医学、薬学、生理学などの分野において、疾患や生理現象の有無や変化を予測するための指標となる数値や物質のことをいいます。 ↩︎
- アポトーシス:細胞自身が引き起こすプログラム細胞死のことで、生命の発生過程で不要な細胞を除去したり、過度のストレス刺激を受けた細胞が周囲に害を及ぼさないように取り除いたりするために引き起こされます。タンパク質分解酵素であるカスパーゼの活性化によって引き起こされ、染色体が凝集して核が断片化し、細胞質も凝集、分断されるという特徴があります。かつては、制御性の細胞死はすべてアポトーシスだと考えられてきましたが、近年の研究で前述のフェロトーシスを始め、アポトーシス以外にもさまざまな制御性細胞死が存在することがわかってきています。 ↩︎
- ネクロプトーシス:上述のアポトーシスを阻害したときに、代わりに生じる制御性の細胞死として報告されました。ネクロプトーシスではアポトーシスと異なり、細胞が膨張して破裂するという、非制御性細胞死であるネクローシスと類似した形態的特徴が示されます。 ↩︎
- 転写因子:遺伝子の発現を調節するタンパク質。転写を活性化するものと抑制するものがあります。 ↩︎
- BACH1:ヘムや酸化ストレス(細胞や生体内で代謝に伴って生じる活性酸素の酸化作用によるストレス。細胞の老化や障害の原因となります。)に応答する転写抑制因子として、酸化ストレス下での細胞の反応に重要な役割を持つことが以前から知られています。2020年に、本研究チームは「BACH1 がフェロトーシスの強力な促進因子である」ことを報告しました。 ↩︎
- 分子標的治療:がんの原因となる遺伝子変異による分子異常を標的とした治療で、従来の殺細胞性抗がん剤による治療と比べて、より少ない副作用で高い効果が得られやすいという特徴があります。 ↩︎
参考文献
1.Fushimi K., et al. Rational conversion of chromophore selectivity of
cyanobacteriochromes to accept mammalian intrinsic biliverdin. ProcNatl Acad Sci U S A 2019; 116:8301-8309.
2.Irikura R., et al. Ferroptosis model system by the re-expression of BACH1. J Biochem 2023; 174: 239-252.
論文情報
タイトル:Intracellular biliverdin dynamics during ferroptosis
著者:Kazuma Nakajima, Hironari Nishizawa, Chen Guan, Shunichi Tsuge, Mie Yamanaka, Machi Kiyohara, Riko Irikura, Mitsuyo Matsumoto, Kozo Tanaka, Rei Narikawa, and Kazuhiko Igarashi
*責任著者: 東北大学大学院医学系研究科 生物化学分野 西澤 弘成、東北大学大学院医学系研究科 生物化学分野 五十嵐 和彦
掲載誌:The Journal of Biochemistry
DOI:10.1093/jb/mvae067
URL:https://academic.oup.com/jb/advancearticle/doi/10.1093/jb/mvae067/7786781
問い合わせ先
(研究に関すること)
東北大学大学院医学系研究科 生物化学分野
教授 五十嵐 和彦 (いがらし かずひこ)
TEL:022-717-7595
Email:igarashi*med.tohoku.ac.jp(*を@に置き換えてください)
東北大学大学院医学系研究科 生物化学分野
非常勤講師 (現:コロンビア大学 Irving がん研究センター研究員[米国])
西澤 弘成(にしざわ ひろなり)
Email:hnishizawa*med.tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院医学系研究科・医学部広報室
TEL:022-717-8032
Email:press*pr.med.tohoku.ac.jp(*を@に置き換えてください)
- 関連資料
- プレスリリース資料(PDF)
- 関連リンク
- 生物化学分野


