加齢による造血幹細胞生着不全の機序を解明 骨髄代謝・血流動態の変容が起因
2025.7.4 Fri
研究発表のポイント
- 白血病などの造血器疾患の根治を可能とする造血幹細胞(HSC)移植の成功率が加齢と共に減少する原因の一端を明らかにしました。
- 骨髄では血球細胞により産生されるアセチルコリンを起点とした一酸化窒素(NO)シグナル経路1によって血流が保たれており、加齢によりその機能低下が見られることが判明しました。
- 骨髄では血流による類洞血管内皮細胞2の活性化により、移植した造血幹細胞(HSC)3の骨髄への生着効率4が維持されていました。
- 高齢個体で低下したHSCの生着効率は、加齢により減弱するNOシグナル経路の再活性化や、骨髄類洞血管の活性化により改善が見込まれる可能性が示されました。
概要
これまでHSC移植時のHSCの生着率は加齢に伴い低下することが知られていましたが、その要因は明らかではありませんでした。
東北大学大学院医学系研究科幹細胞医学分野および国立健康危機管理研究機構 国立国際医療研究所 造血システム研究部の田久保 圭誉教授・部長、同部の森川 隆之上級研究員ら、神奈川県立産業技術総合研究所の研究グループは、この要因として骨髄の局所血流・代謝に着目し、加齢による血流の減少に加え、血管拡張を担うアセチルコリンや一酸化窒素(NO)を介するシグナル経路の減弱を認めました。このとき血液と血管壁の間に血流によって生じる力であるずり応力5も、骨髄類洞血管で加齢により低下することがわかりました。HSCの骨髄への生着におけるずり応力の役割を検証したところ、移植後HSCの生着効率の加齢による低下は、アセチルコリン-NOシグナル経路の加齢変化が一因であることが示されました。同シグナル経路が高齢個体での移植効率の改善に向けた有効な治療標的となりうることが期待されます。
本成果は、2025年7月1日付で学術誌Nature Communicationsに掲載されました。
詳細な説明
研究の背景
造血幹細胞(HSC)移植は白血病などの造血器疾患の根治を可能とする重要な治療法のひとつであり、日本だけでも毎年6000件近くの移植が行われています。しかしながら、未だ造血幹細胞移植の適応年齢は限られており、加齢とともに増加する造血器腫瘍のリスクに十分に対応出来ているとは言い難いのが現状です。その要因としては、高齢者における移植関連合併症に加え、移植した造血幹細胞の骨髄への移行・生着の効率が加齢とともに減少していくことなどが挙げられます。したがって造血幹細胞の生着のメカニズムの解明や、その加齢に伴う生着効率の低下要因の探索は、年々その進行が予測されている高齢化社会での造血器疾患治療における取組として必須の課題であるといえます。この生着の過程における移植された造血幹細胞の骨髄血管外遊走にはさまざまな接着分子や細胞走化性因子が関与しているとされますが、炎症組織でのリンパ球の血管外遊走で知られているような血流動態の重要性は明らかではありませんでした。
今回の取り組み
東北大学大学院医学系研究科幹細胞医学分野および国立健康危機管理研究機構 国立国際医療研究所 造血システム研究部の田久保 圭誉(たくぼ けいよ)教授・部長、同部の森川 隆之(もりかわ たかゆき)上級研究員ら、神奈川県立産業技術総合研究所の研究グループは、加齢による骨髄の血流動態の変容のメカニズムに着目し、それらの造血幹細胞の生着における役割を明らかにすることを目指しました。さらにそこから得られた知見をもとに血流によって変化を生じる因子群を標的とし、それらに介入を加えることで加齢個体における生着率を効率的に改善する治療法の確立に挑みました。
まず研究グループは、加齢による骨髄微小環境の変化を明らかにするため、若齢マウスと加齢マウスの骨髄の代謝をメタボローム解析により比較しました。すると若齢マウスと比較して高齢マウスでは血流維持に重要な、アセチルコリンを起点とし一酸化窒素(NO)を介したシグナルに関わる代謝物の低下(図1)や、血流低下を示すグルコース代謝産物、アミノ酸などの減少が認められました。これらの結果を踏まえ、高齢マウスと若齢マウスの骨髄の血流動態を、生体顕微鏡6を用いて測定したところ、加齢による骨髄の血流の低下が認められました(図2)。そこでこの加齢による骨髄血流低下の原因を探るために、アセチルコリンの合成系と分解系の加齢変化を調べました。するとアセチルコリンの合成を担うコリンアセチル転移酵素は主に骨髄ではB細胞で発現していましたが、その加齢変化は認められませんでした。一方でアセチルコリンの分解を司るコリンエステラーゼの活性が若齢と比較して高齢マウスでは高いことがわかりました。これらの結果からNOシグナル経路は骨髄血流を保つために重要な役割をしており、加齢による同経路の機能低下によって骨髄の血流が減少していることが示されました。この血流によって血液と血管壁との間にずり応力と呼ばれる力が生じていますが、これを血管内皮細胞上のメカノセンサーPiezo17が感知することで血管構造の変化が促され、血管壁を通過してリンパ球が血管外へと遊走することが知られています。加齢マウスでは、このずり応力も骨髄の類洞血管血流の低下に一致して若齢マウスと比べて減少していました。一方で骨髄中の血管内から骨髄実質へのHSCの遊走は移植したHSCが生着するための重要なプロセスのひとつです。そこで血流中の造血幹前駆細胞(HSPC)の骨髄実質への移行しやすさの指標となる、HSPCが類洞血管壁の通過にかかる時間Δtを、生体顕微鏡を用いて高齢マウスと若齢マウスで比較しました。すると、高齢マウスではHSPCは血管壁通過に若齢マウスの2倍以上の時間がかかり、HSPCが血流中から骨髄実質への移行する効率が加齢によって低下していることが示唆されました。またこの加齢によるHSPCの移行効率の低下は骨髄局所へのNO添加や、Piezo1活性化剤の添加などによって改善が見られました (図3)。これらの結果から、NOシグナル経路によって保たれている骨髄の血流により、HSPCの血管外遊走能が維持されており、加齢によるこのメカニズムの低下がHSCの生着効率の低下の一因となっている可能性が示唆されました。さらに骨髄のNO-Piezo1を介した同経路が、加齢個体におけるHSCの骨髄への移行効率改善の治療標的となりうるかを探るため、加齢マウスにHSC移植をおこない、NOシグナル経路や、Piezo1を活性化することで移植効率が改善するかを検証しました。まず高齢マウスに移植したHSCの短期の骨髄への移行を精査したところ、加齢によって低下したHSCの移行効率はNO投与 やPiezo1の活性化剤の投与により改善が見られました (図4)。また長期ではHSC移植後の高齢マウスの生存率が、Piezo1活性化剤の投与により改善しました (図5)。これらの結果から骨髄では血球系から産生されるアセチルコリンを起点としたNOシグナル経路によって血流が保たれており、HSCの骨髄への移行が担保されていることが示唆されました。また加齢による同シグナル経路の減弱によりHSCの骨髄移行効率が低下しており、これを抑制することで高齢でのHSC移植効率が改善される可能性が示されました(図6)。
今後の展開
今回示された知見から、骨髄の血流がHSCの骨髄への生着に関わる因子であることが新たに示されました。一方でどのような機序で加齢によって骨髄中のアセチルコリンの分解系が亢進するかなどまだ十分に明らかになってはおらず、骨髄以外のアセチルコリン代謝系の加齢変化などとの連関なども考慮しながら解明してくことなどが今後の課題のひとつとなっています。さらに、今回の知見の臨床応用の可能性などを鑑みると、骨髄局所でのNOシグナル経路の活性化や、Piezo1の活性化の手段などがハードルとなることも予想されることから、研究グループはこうした課題の克服を目指した取り組みを続けています。
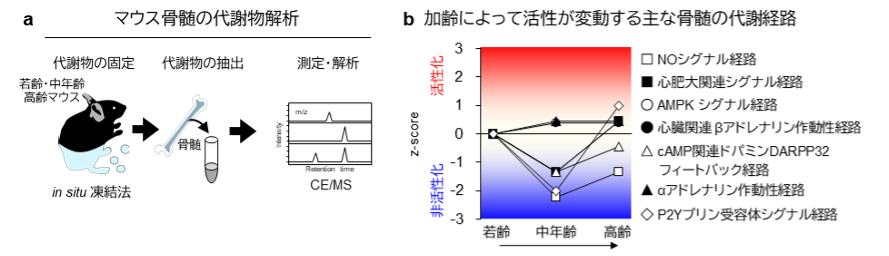
a マウス骨髄の代謝物解析の流れ。代謝物の分解が少ないin situ凍結法によって得られた骨髄サンプルから代謝物を抽出しキャピラリー電気泳動/質量分析計(CE/MS)により各代謝物の骨髄内濃度を測定しました。
b 代謝物測定値から加齢によって変動が予測された代謝経路。NOシグナル経路が加齢によって活性が低下する代謝経路のひとつとして示されました。
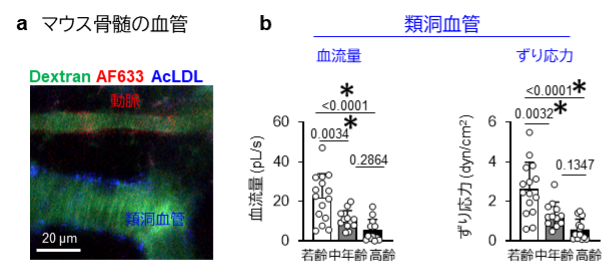
a マウス骨髄の血管の生体顕微鏡画像。蛍光色素を結合させたデキストランで血管を描出し (緑)、動脈のマーカーAF633 (赤) と類洞血管のマーカーAcLDL (青) でそれぞれの血管を識別しました。
b 加齢による類洞血管の血流量とずり応力の変化。類洞血管では血流の低下とともに、ずり応力も加齢によって減弱していました。
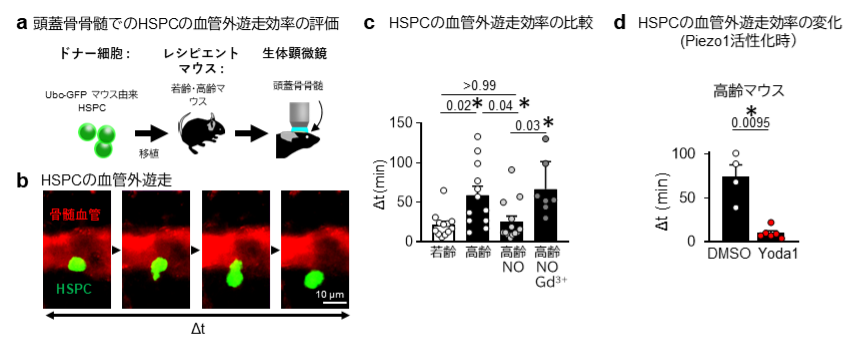
a HSPCの血管外遊走効率の評価方法。緑色蛍光色素GFPを全身で発現するUbc-GFPマウス由来のHSPCをマウスに移植し、頭蓋骨骨髄での血管外遊走に要する時間を測定しました。
b 頭蓋骨骨髄のHSPCの血管外遊走の様子。血流に乗って骨髄に到達したHSPCの類洞血管壁接着から血管壁を通り抜けるまでの時間Δtを血管外遊走効率の指標として用いています。Δtの値が小さいほど効率よく血管外遊走が起きていると考えられます。
c HSPCの血管外遊走効率の比較。若齢マウスと比較して高齢マウスではHSPCの血管外遊走にかかる時間が2倍以上に延長しており、加齢による遊走効率の低下がうかがえます。この加齢によるΔtの延長はNOの投与により短縮し、またPiezo1の阻害剤であるガドリニウム(Gd3+)により再び延長しました。
d Piezo1活性化によるHSPC血管外遊走効率の変化。Piezo1の活性化剤Yoda1投与により高齢マウスで低下したHSPCの血管外遊走の効率の回復が認められます。DMSO:コントロール群。
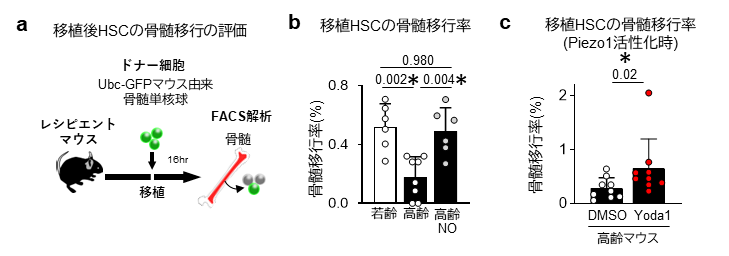
a 移植後短期でのHSCの骨髄移行の評価。Ubc-GFP由来の骨髄単核球をマウスに移植し、16時間後レシピエントマウス骨髄中のドナーマウス由来のHSCの割合をフローサイトメーターで測定しました。
b 移植HSCの短期骨髄移行率。加齢より低下した移植HSCの骨髄移行率はNO投与により回復しました。
c Piezo1活性化時の高齢マウスの移植後HSCの骨髄移行効率。高齢マウスのHSC骨髄移行効率はコントロール群 (DMSO) と比較してPiezo1活性化時 (Yoda1) で上昇しました。
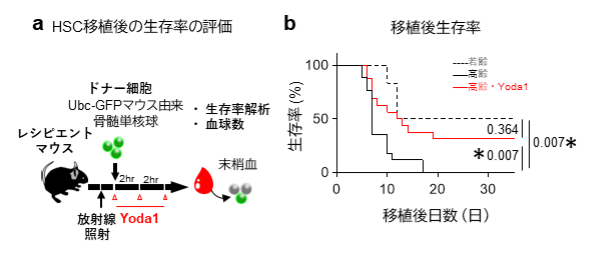
a HSC移植後の生存率の評価方法。レシピエントマウスへの放射線照射後、Ubc-GFPマウス由来の骨髄細胞を移植し、1か月にわたって末梢血の回復をモニターしながら生存率を比較しました。
b 若齢マウス、高齢マウス、高齢マウスのYoda1投与群のHSC移植後の生存曲線。若齢マウスと比較して低下した高齢マウスの生存率は、Yoda1投与で回復しました。
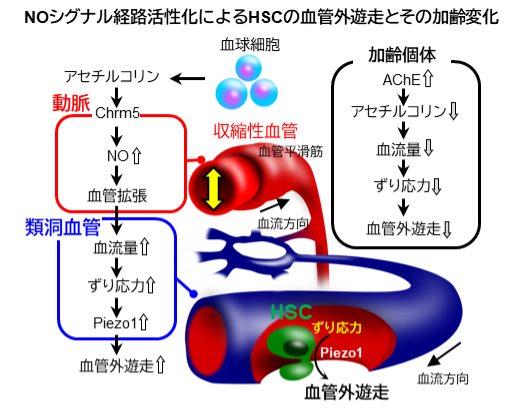
骨髄の血球細胞が産生するアセチルコリンは動脈血管内皮細胞上のアセチルコリン受容体 (Chrm5) を介してNO産生を促します。NOによる動脈径の拡張は、下流の類洞血管の血流量の増加及びずり応力を増加させ、これを感知したPiezo1の活性化よりHSCの血管外遊走が促されます。加齢による骨髄のアセチルコリンの低下はこのカスケードの機能を減弱させ、HSCの効率的な血管外遊走が妨げられると考えられます。
謝辞
本研究は以下の研究資金・枠組みによる支援のもと行われました。
・日本医療研究開発機構(AMED):
先端的な遺伝子・細胞治療技術の開発JP18ae0201014
分子基盤に基づいた革新的がん診断・創薬等の開発に関する研究JP18ck0106444
幹細胞・再生医学イノベーション創出プログラムJP20bm0704042,
革新的先端研究開発支援事業(AMED-CREST):
「生体組織の適応・修復機構の時空間的解析による生命現象の理解と医療技術シーズの創出」研究開発領域JP20gm1210011
「根本的な老化メカニズムの理解と破綻に伴う疾患機序解明」研究開発領域 JP24gm6710025
ムーンショット型研究開発事業JP22zf0127007
・神奈川県立産業技術総合研究所(KISTEC)戦略的研究シーズ育成事業
・文部科学省・日本学術振興会(JSPS)科学研究費補助金:
JP19K17847, JP21K08431, JP19K17877, JP21J01690, JP22K08493, JP18H02845, JP20K21621, JP21H02957, JP 22K19550, 24H00640, 25H01435, 18K08379, 21K08383, 24K11529, 25K19565, 24K11551
・文部科学省世界トップレベル研究拠点プログラムWPI-Bio2Q
・文部科学省共同利用・共同研究拠点「マルチオミックスによる遺伝子発現制御の先端的医学共同研究拠点」(横浜市立大学先端医科学研究センター)
・国立国際医療研究センター国際医療研究開発費
・武田科学振興財団助成金
・化血研ステップアップ研究助成
・中冨健康科学振興財団 研究助成金
用語説明
- 一酸化窒素 (NO) シグナル経路:動脈系においてはアセチルコリンなどによって血管内皮細胞のNO合成酵素が活性化しNO産生が上昇します。NOが内皮細胞に近接した血管平滑筋細胞を弛緩させることで血管が拡張します。 ↩︎
- 類洞血管 : 骨髄の血管の中で上流側の動脈などと比較して径が太く、下流側にあたる血管です。主にこの類洞血管の壁を介して血球細胞や物質が血管内外の行き来をしているとされます。 ↩︎
- 造血幹細胞 : 分裂することで生涯にわたってあらゆる血液細胞を供給している細胞です。哺乳動物の成体では主に骨髄に存在している数少ない細胞です。 ↩︎
- 生着 : 造血幹細胞移植において、移植した造血幹細胞が血中から骨髄に移行したのち、造血を開始することを生着と言っています。 ↩︎
- ずり応力:血液循環系においてずり応力とは血流が血管壁に平行な方向に作用する力で、流速が速いほどずり応力は大きくなります。 ↩︎
- 生体顕微鏡 : 麻酔など適切な処置をした個体の生体機能を保ったまま各臓器などの詳細な画像情報を取得することを目的とした顕微鏡が生体顕微鏡です。本研究のように高速で骨髄深部の画像を繰り返し取得できる多光子レーザー顕微鏡システムを用いることで、骨髄内の組織学的な情報の取得はもとより、血管内の赤血球速度や血中赤血球密度を測定することで血流やずり応力などの算出などが可能となっています。 ↩︎
- Piezo1:ずり応力など機械刺激により作動し、細胞内シグナルなどを活性化する膜タンパク質です。血管内皮上のPiezo1はずり応力を感知して血管内皮細胞どうしの接着を調節していることなどが報告されています。 ↩︎
論文情報
タイトル:Decreased non-neurogenic acetylcholine in bone marrow triggers age-related defective stem/progenitor cell homing
著者:森川隆之、藤田進也、杉浦悠毅、玉置親平、原口美帆、城下郊平、綿貫慎太郎、小林央、須藤光、内藤善子、早川典代、松浦友美、菱木貴子、松井稔、筒井正人、末松誠、田久保圭誉*
*責任著者:
東北大学大学院医学系研究科幹細胞医学分野 教授
国立健康危機管理研究機構 国立国際医療研究所 造血システム研究部長
田久保 圭誉
掲載誌:Nature Communications
URL:https://www.nature.com/articles/s41467-025-60515-9
問い合わせ先
(研究に関すること)
東北大学大学院医学系研究科幹細胞医学分野
教授 田久保 圭誉(たくぼ けいよ)
TEL:022-717-8150
Email:keiyo.takubo.e5*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院医学系研究科・医学部広報室
TEL:022-717-8032
Email:press.med*grp.tohoku.ac.jp(*を@に置き換えてください)
- 関連資料
- プレスリリース資料(PDF)
- 関連リンク
- 幹細胞医学分野


