発表のポイント
- 歯を構成する象牙質やセメント質における石灰化は、DNAの塩基配列を変えずに細胞が遺伝子の働きを調整する後天的な機構(エピジェネティクス)1によって制御されていることが明らかになりました。
- エピジェネティクスに重要なヒストン脱アセチル化酵素(HDAC)2の機能を抑制した遺伝子改変マウスでは、臼歯の歯根が短くなり、神経や血管が通る歯根尖の孔(根尖孔)が早期に閉鎖されることがわかりました。
- 本研究成果は、将来的に再生歯胚における歯根形態の人為的制御技術に応用され、歯の再生の実現につながることが期待されます。
概要
歯の再生は夢の治療法です。しかし、再生された歯の形態、特に歯根の長さや構造を制御する技術は、未だ十分に確立されていません。
東北大学大学院歯学研究科分子・再生歯科補綴学分野の新部邦透講師および江草宏教授らは米国Mayo Clinicとの共同研究により、エピジェネティクス因子として知られるヒストン脱アセチル化酵素(HDAC3)の発現を欠失させた遺伝子改変マウスの歯を解析しました。その結果、同マウスでは歯根の長さが短縮し、神経や血管の通る歯根尖の孔(根尖孔)が通常よりも早期に閉鎖されることが明らかとなりました。加えて、HDAC3の発現を阻害する薬剤を処理したセメント芽細胞3において、石灰化に関連する遺伝子の発現が抑制され、実際の石灰化も抑制されることが細胞レベルで確認されました。
これらの成果は、将来、歯胚再生技術の実用化が進んだときに、歯根形態を制御するための新たな技術基盤として活用されることが期待されます。
本研究成果は、2025年8月23日付で骨代謝の専門誌Journal of Bone and Mineral Researchオンライン版に掲載されました。
詳細な説明
研究の背景
夢の治療である歯の発生の元となる「歯胚」の再生をめぐる基礎研究は着々と進んでいます。しかしながら、試験管内で誘導された再生歯胚の形態は制御することが難しく、どのような大きさ、形態となるかは成長させてみないと分からないのが現状です。これまで、歯の形態を制御するために、人為的に形態を付与した三次元の枠を用いることや、歯の元となる細胞の遺伝子発現を制御して、細胞の分化や石灰化度をコントロールすることが試されてきました。
今回の取り組み
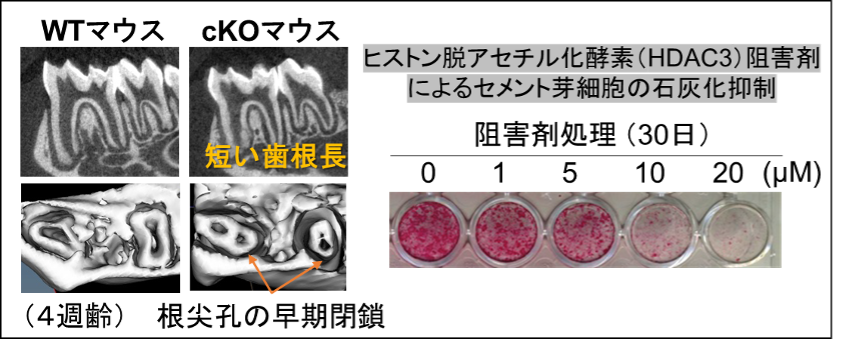
今回、東北大学大学院歯学研究科 分子・再生歯科補綴学分野の新部邦透(にいべ くにみち)講師および江草宏(えぐさ ひろし)教授、ならびに米国Mayo Clinic整形外科のJennifer J. Westendorf教授らの研究グループは、硬組織特異的に発現する遺伝子であるOsterix4が発現した細胞で、エピジェネティクス因子として知られるヒストン脱アセチル化酵素(HDAC3)の発現が欠失するマウス(cKOマウス)の歯を解析したところ、野生型マウス(WTマウス)と比較して歯根の長さが短くなり、歯根尖にある神経や血管の通る孔が早期閉鎖することを見出しました(図1:左)。また、cKOマウスから採取した歯髄細胞の石灰化も抑制されました。さらに、HDAC3の発現抑制薬(阻害剤)を用いてセメント芽細胞に処理を行ったところ、細胞の石灰化を抑制することに成功しました(図1:右)。
今後の展開
本技術は、試験管内で誘導された歯胚の歯根成長を遺伝子操作することなく人為的に操作し、必要な長さを超えないよう制御する技術に応用できる可能性や、歯原性細胞の新たなエピジェネティクス制御性の発見につながる可能性があります。
謝辞
本研究は、JSPS科研費 基盤C(19K10220)、国際共同研究加速基金(17KK0182)、JST創発研究(JPMJFR2210)、NIH grant (T32056950)、Mayo Clinic Foundationの一環で行われました。
用語説明
- エピジェネティクス:DNAの塩基配列の変化を伴わずに、細胞分裂後も継承される遺伝子発現や細胞表現型の変化で「後成学」、「後成遺伝学」と言われる。DNAの塩基配列の変化しない遺伝子のオン・オフを制御するDNAの化学的修飾で、先天的な要因のほか、環境因子である生活環境や生活習慣、栄養状態、ストレスなどにより影響を受ける。 ↩︎
- ヒストン脱アセチル化酵素(HDAC):DNAとタンパクの複合体であるクロマチンは、ヒストン8量体にDNAが巻き付いたヌクレオソーム構造を形成し、ヌクレオソームが連なり、クロマチン繊維、高次のクロマチン構造を形成する。ヒストン脱アセチル化酵素は、このクロマチンの構成要素であるヒストンを脱アセチル化する酵素で、巻き付いたDNAの塩基配列に関する遺伝子の転写を制御している。HDACにはI, II, IIIの3つのファミリーが存在する。 ↩︎
- セメント芽細胞:歯の歯根表面に存在するセメント質を形成する細胞。自身の周りにセメント質を形成するとセメント室に埋もれてセメント細胞となる。 ↩︎
- Osterix遺伝子:SP7/Osterix遺伝子は、骨形成、骨の基質を作る骨芽細胞の分化に重要な転写因子として知られている。近年では、骨だけではなく、歯に関わる硬組織である象牙質やセメント質の元となる細胞でも発現しており、分化や石灰化に関わっていることが分かっている。 ↩︎
論文情報
タイトル:Inhibition of histone deacetylase 3 in dental mesenchyme regulates the development of tooth root
著者:Kunimichi Niibe*, Dana L. Begun, Kanna Doi-Fujimura, Atsuhiro Nagasaki, Elizabeth Zars, Xiaodong Li, Earnest L. Taylor, Mary B. MacDougall, Hiroshi Egusa, and Jennifer J. Westendorf*
*責任著者:東北大学大学院歯学研究科 講師 新部邦透、Mayo Clinic 教授Jennifer J Westendorf
掲載誌:Journal of Bone and Mineral Research
DOI:https://doi.org/10.1093/jbmr/zjaf102
問い合わせ先
(研究に関すること)
東北大学大学院歯学研究科 分子・再生歯科補綴学分野
講師 新部 邦透(にいべ くにみち)
TEL:022-717-8363
Email:kunimichi.niibe.d4*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院歯学研究科 広報室
TEL:022-717-8260
Email:den-koho*grp.tohoku.ac.jp(*を@に置き換えてください)
- 関連資料
- プレスリリース資料(PDF)
- 関連リンク
- 咬合修復科


