有望な骨補填材の骨再生力を増強 ―リン酸八カルシウム/ゼラチン/ コラーゲン様ペプチド組成が骨形成を促進―
2026.3.27 Fri
研究発表のポイント
- 整形外科領域で骨補填材1として臨床応用されているリン酸八カルシウム2/ゼラチン3複合体(OCP/Gel)に、コラーゲン様ペプチド(CMP)4を複合化することで骨再生5能を増強させることを見出しました。
- OCP/Gelは、東北大学で開発され、OCPが有する生体材料の特性により、生体吸収性6および新生骨への置換性が確認された材料です。
- 自家骨が示す高い骨再生能獲得を目標として研究を継続して、OCP/Gelの新たな複合組成(OCP/Gel/CMP)による骨形成の促進を明らかとし、その細胞・分子レベルのメカニズムを提案しました。
概要
自己修復が困難な骨欠損を治療するために、自家骨に代わる安定供給可能な人工材料が開発されていますが、その適用の拡大には骨再生能の増強が課題とされています。
東北大学大学院歯学研究科(生体材料理工学分野)の濱井瞭講師、土屋香織学術研究員、鈴木治教授、同大医学系研究科(整形外科学分野)の原田健登大学院生、森優講師、金淵龍一助教、相澤俊峰教授らの研究グループは、北海道大学大学院歯学研究院(硬組織微細構造学教室)の長谷川智香准教授、網塚憲生教授と共同で、OCP/Gel/CMPの骨再生がどのように生じているかを研究し、その発現メカニズムを提案しました。
Gelの部位に、コラーゲンよりも小さい分子であるCMPを複合化すると、OCP の存在下でGel表面での骨芽細胞7による骨基質石灰化8が促進され、それにより複合体の骨再生能自体も増大することが明らかとなりました。研究グループは、OCP自体の骨再生能の増大法も並行して研究しており、今回、OCPを混合する材料側(Gel)による骨形成促進が確認でき、OCP/Gel/CMP材料は次世代型骨補填材としての臨床応用が期待されます。
本成果は、2026年3月25日に生体材料科学分野の国際誌Acta Biomaterialiaにオンライン速報版として掲載されました。
詳細な説明
研究背景
疾病や外傷で失われ、自己修復が難しい骨欠損を修復するために、人工材料を充填する補填治療が広く行われていますが、第一の選択としては高い自己再生能を持つ自身の骨である自家骨が使用されています。ただし自家骨採取は二次侵襲を伴ううえに、量的な制限もあることが問題とされています。
そのため、自家骨に代わり安定供給が可能で生体親和性が高く、骨に直接結合可能な骨伝導性9を示す人工材料の開発が求められてきました。代表的な材料として、ハイドロキシアパタイト(HA)10や、破骨細胞11の作用により生体内で吸収性を示すβ-リン酸三カルシウム(β-TCP)12といったリン酸カルシウム系材料が広く臨床応用されています。ただしこれらの人工材料は骨伝導性を示すものの、自家骨と比較すると、新たな骨組織(新生骨)を形成して骨を再生する能力は限定的であるため、より高い骨再生能を持つ人工材料の開発が検討されてきています。
本研究グループは、骨や歯のアパタイト結晶の前駆体として知られている無機物質のリン酸八カルシウム(OCP)に着目しました。研究グループは1991年より、生体材料として使える十分量のOCPを均質に人工合成することを実現し、OCPがHA材料と比較してより早い骨形成を引き起こすこと、またβ-TCP材料と比較してより高い生体内吸収性を有することを解明してきました。これらの研究成果を基に、近年、東北大学発の骨補填材として、歯科領域でOCP/コラーゲン複合体、また、整形外科領域でOCP/ゼラチン(OCP/Gel)複合体が社会実装されました。Gelはコラーゲン由来の熱変性産物で水溶性(親水性)をもちます。一方、コラーゲンは不溶性を示し、生理的環境下で安定して存在します。これら、OCP骨補填材は、臨床の現場で実際に骨を再生する材料として複数の論文報告がなされています。
今回の取り組み
本研究グループは、OCP骨補填材のさらなる骨再生能の増大を目標として、Gelの中にコラーゲンよりも小さい分子であるCMPを複合化してOCP/Gel/CMPを創製しました。
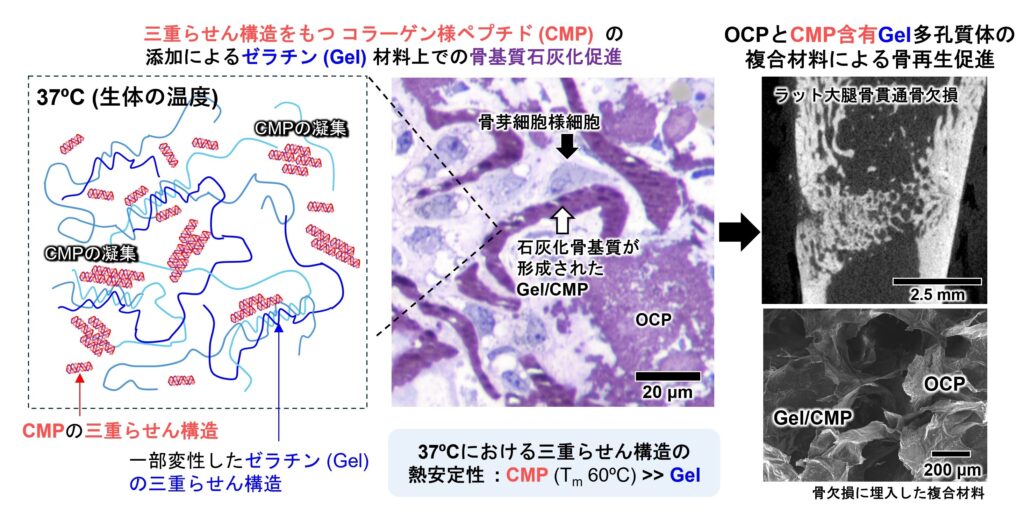
図1のμCT像に示すように、GelにCMPを添加し、その上でOCPの顆粒と共に成型したOCP/Gel/CMPは、ラット大腿骨の皮質骨貫通欠損で新生骨形成を促進し、CMPを含まない従来のOCP/Gelと比較して4週間埋入した新生骨量が1.6倍ほど高くなり、骨形成が有意に(p<0.05)促進されることがわかりました。
不溶性であるコラーゲンの三重らせん構造は、骨組織の石灰化(リン酸カルシウム形成)開始に関与していると考えられています。本研究で用いられたCMPの組成は、(Gly-Pro-Hyp)10であり、コラーゲンよりも短い分子ですが、コラーゲンの三重らせん構造を生理的温度以上でも保持するタイプの分子として知られています。図1のGel /CMPの分子構造概念図に示すように、CMPは互いに凝集するように存在しています。このことから、三重らせん構造がほとんど解けているGelの分子にも親和性を示して相互作用している、いわば、Gelとコラーゲンの中間状態のような新規な材料構成が創出されていると推察されます。
また、OCPとCMP/Gelが共存するMSCの細胞凝集塊(スフェロイド)13 を14日間培養し、von Kossa染色を行ったところGel/CMPの骨基質石灰化がGelと比較して有意に(p<0.01)促進されることが明らかになりました。また、培養7日後のスフェロイドの電子顕微鏡観察により、Gel/CMPにおいてナノサイズのリン酸カルシウム針状結晶が高密度で化学的に析出した部位において、MSCから分化した骨芽細胞による骨基質の分泌とその石灰化が開始することが確認されました。一方でGel表面では、骨芽細胞の骨基質の分泌は認められるものの、その石灰化には至っていませんでした。
Gelとコラーゲンの中間状態のような材料構成では、Gelの親水性の高さにより、OCPから溶出したカルシウムイオンとリン酸イオンがGel/CMP材料内部まで浸透しやすく、これらイオンを原料としてCMPの三重らせん構造の存在に関連してリン酸カルシウム針状結晶が析出したと考えられます。針状結晶の析出は、OCPとともに周囲のイオン濃度を変化させてMSCの骨芽細胞への分化を促すだけでなく、このような結晶が析出したGel/CMPの部位は、骨芽細胞の成熟化とともに骨基質石灰化に最適な足場として骨形成促進に関与している可能性が細胞の遺伝子解析ならびに培地の化学分析、材料と細胞の電子顕微鏡観察などから示唆されました。
以上から、CMPをOCP/Gelに添加することで、Gel/CMPのリン酸カルシウム針状結晶析出部位上で骨芽細胞が骨の有機質であるコラーゲンの分泌だけでなくその石灰化を早期に開始し、結果としてOCP/GelよりもOCP/Gel/CMPで骨形成が増大するというメカニズムを提案しました。
今後の展望
研究グループは、OCP自体の一連の材料特性の調節による骨再生能の増強も並行して研究しており(参考文献1)、今回の成果と融合して、次世代型のOCP骨補填材における将来の臨床応用可能性を検討していく予定です。
謝辞
本成果の研究は、科学研究費補助金(日本学術振興会科研費JP21K19586, JP21H03121, JP23K08604, JP24K02624)の研究助成等の支援を受けて行われました。
参考文献
1.Acta Biomater 158:1-11, 2023(DOI: 10.1016/j.actbio.2022.12.046)
用語説明
- 骨補填材:疾病や事故で生じた骨の治療や再生において、骨欠損を補填する材料である。日本では患者自身から採取した正常部位の骨組織(自家骨)や、顆粒状やブロック状、スポンジ状といった形態をもつ人工骨が使用されている。OCPにおいては、形状付与による操作性向上の観点から、これまでにコラーゲン、ゼラチン、アルギン酸、ヒアルロン酸、乳酸-グリコール酸共重合体といった生体吸収性高分子材料との複合化が検討され、その骨補填材としての性質や機能がこれまでに研究されてきた。OCPとコラーゲンの複合体は歯科領域で、OCPとゼラチンの複合体は整形外科領域で、骨補填材として実用化されている。 ↩︎
- リン酸八カルシウム (OCP) :化学式はCa8H2(PO4)6・5H2Oと表記され、水溶液中からのHA(*10)形成の前駆体の一つであり、また、骨アパタイト結晶の前駆体とも考えられてきた生体材料である。リン酸オクタカルシウムとも称されている。化学式が示す通り、多量の水を含むため、HAやβ-TCP(*12)と異なり、単一結晶相として焼結できないことから、生体由来高分子、天然由来高分子、合成高分子と組み合わせた複合体の研究が報告されている。β-TCPと同様に生体内吸収性を示す。また、OCPは骨芽細胞など、骨組織に関連するいくつかの細胞を活性化する能力を持つことが報告されている。 ↩︎
- ゼラチン(Gel):コラーゲンの熱変性産物である。コラーゲンは不溶性であるが、ゼラチンは、ある温度以上ではコラーゲンに特徴的な分子鎖の三重らせん構造がほどけた状態であることから、水に溶けやすい。一方で、ゼラチン水溶液をある温度以下で冷却すると、一部の分子鎖がコラーゲンに類似の三重らせん構造を取り、ゲル化する。ゼラチンは、細胞接着性を示すとともに、生体内の酵素によって分解されることから生体吸収性を示し、ゲル化する性質を材料加工に利用することで、組織再生における足場材料としての応用も検討されている。 ↩︎
- コラーゲン様ペプチド(collagen mimetic peptide; CMP):コラーゲン様ペプチド(CMP)は、コラーゲンに特徴的な三重らせん構造を形成するように人工的に設計・合成された分子である。CMPは、天然のコラーゲンよりも小さい分子である。複数のアミノ酸が化学的に結合(ペプチド結合)して連なった鎖状の分子であり、これら分子鎖が3本集まって、三重らせん構造を形成し、さらに線維化したものが生体のコラーゲンである。この鎖状の分子は、Gly-X-Yを基本単位としたアミノ酸配列が繰り返し連なっている。Glyはグリシンであり、XとYには、様々なアミノ酸が配列するが、XにはPro (プロリン)、YにはHyp (ヒドロキシプロリン)が多く存在する。特に、Hypが三重らせん構造の形成に重要な役割をもつ。代表的なコラーゲン様ペプチドの一つに、(Gly-Pro-Hyp)nがあり、基本のアミノ酸配列の繰り返しの数 (n) が大きいほど、三重らせん構造の熱的安定性が高い傾向にある。 ↩︎
- 骨再生:疾病や怪我で失われた骨は、その欠損サイズが小さければ自然に骨が再生され元にもどるが、大きな欠損は自己修復できないことが知られている。そのため、自家骨移植や人工材料を補填した骨再生治療が行われている。 ↩︎
- 生体吸収性:材料が自身の物理化学的性質や、周囲の細胞が分泌する酵素の作用によって生体内で溶解もしくは分解され、吸収される性質である。OCPは、骨を造る細胞である骨芽細胞の活性化のみならず、骨組織の吸収にかかわる破骨細胞の形成を促進することから、これらの細胞によって、生体内で分解、吸収されるとともに、新しい骨組織に置き換わる性質を示す。 ↩︎
- 骨芽細胞:骨芽細胞は骨組織の形成を担う細胞である。 ↩︎
- 骨基質石灰化:骨は、リン酸カルシウムの一種であるハイドロキシアパタイト(HA)を基本型とする無機質の骨アパタイト結晶とタンパク質の一種であるコラーゲンを主体とする有機質から構成される組織である。骨芽細胞により骨組織がつくられる際、リン酸カルシウムが形成される過程を石灰化という。骨芽細胞は、コラーゲンの線維形成に加え、脂質の膜からなる袋状の粒子である基質小胞を分泌する。基質小胞では、その内部にカルシウムイオンや無機リン酸イオンが流入してリン酸カルシウムが析出し、膜を突き破るように結晶が成長する。この結晶 (石灰化球) の形成過程は基質小胞性石灰化とよばれている。この石灰化球がコラーゲン線維に接触することで、コラーゲンの三重らせんに沿うようにリン酸カルシウムが形成されていく。この過程はコラーゲン性石灰化とよばれている。 ↩︎
- 骨伝導性:骨欠損に材料を埋入した際、その表面に直接、骨芽細胞の作用によって新生骨組織が形成され、材料が線維性組織を介さずに骨組織と結合する性質を指す。 ↩︎
- ハイドロキシアパタイト(HA):化学式は Ca10(PO4)6(OH)2と表記される。骨アパタイトは、HAを基本型とし、その組成は炭酸イオンやマグネシウムイオンなどいくつか他の成分を含んだ、炭酸含有カルシウム欠損型のアパタイトであることが知られている。人工合成の HA を高温で焼結したセラミックス材料は、骨伝導性を示し、骨補填材として臨床応用されている。 ↩︎
- 破骨細胞:破骨細胞は骨吸収を担う細胞である。 ↩︎
- β-リン酸三カルシウム(β-TCP):化学式はβ-Ca3(PO4)2 と表記され、HAセラミックスと同様に高温で焼結した材料が骨補填材として臨床応用されている。骨伝導性と生体内吸収性を示す。
↩︎ - 細胞凝集塊 (スフェロイド):通常、細胞を培養皿で培養すると(2次元培養)、細胞はその表面に接着して増殖することで、平面状に分布する。一方で、細胞接着性を示さない基材上や培地に浮遊するように培養すると(3次元培養)、細胞同士が接着するととともに増殖して、厚みのある球状の塊を形成する。この細胞が集まった塊は、細胞凝集塊(スフェロイド)とよばれ、平面に培養された細胞と比較すると生体により類似した状態にあることから、薬剤や材料への細胞の反応を解析するためのモデルなどにも応用されている。 ↩︎
- 間葉系間質細胞:間葉系間質細胞は骨芽細胞に分化する。 ↩︎
論文情報
タイトル:Addition of a collagen mimetic peptide to octacalcium phosphate/gelatin composites enhances bone formation by accelerating calcification
著者:Kento Harada, Ryo Hamai, Yu Mori, Tomoka Hasegawa, Ryuichi Kanabuchi, Kaori Tsuchiya, Norio Amizuka, Toshimi Aizawa, and Osamu Suzuki*
*責任著者:東北大学大学院歯学研究科 生体材料理工学分野 教授 鈴木 治
掲載誌:Acta Biomaterialia 2026 in press
DOI:10.1016/j.actbio.2026.03.043
URL:https://www.sciencedirect.com/science/article/pii/S174270612600190X
問い合わせ先
(研究に関すること)
東北大学大学院歯学研究科生体材料理工学分野
教授 鈴木 治
Email:suzuki-o*tohoku.ac.jp(*を@に置き換えてください)
(報道に関すること)
東北大学大学院歯学研究科広報室
TEL:022-717-8260
Email:den-koho*grp.tohoku.ac.jp(*を@に置き換えてください)
- 関連資料
- プレスリリース資料(PDF)


